Что такое супрессия костного мозга
Химическая и лекарственная апластическая анемия — лекарства поражающие костный мозг
Апластическая анемия, обусловливаемая химическими и физическими агентами характеризуется прямым отношением количества воздействующего на костный мозг токсического вещества и интенсивности развиваемой им гипоплазии (Мунтяну, Rohr); наличием — в клинической картине — отдельных признаков поражения участков паренхимы органов большого значения, таких как печень, почки, центральная нервная система, что реже наблюдается при остальных видах апластической анемии.
К токсическим веществам, оказывающим большое влияние на костный мозг и очень хорошо изученным, относятся бензол, хлорамфеникол и ряд других медикаментов.
Ниже приведены вещества, определяющие гипоплазию костного мозга и оценка представляющего ими риска.
Физические и химические факторы, обусловливающие развитие апластической анемии:
А. Факторы, наличие которых в определенном количестве, в любом случае способствуют развитию аплазии костного мозга, в том числе, ионизирующие излучения, соединения иприта (азотный иприт и пр.), цитостатические медикаменты (антиметаболиты, антифолиевые препараты), бензол, его соединения.
Б. Факторы, вызывающие лишь случайно костномозговую аплазию, в том числе:
1. Противомикробные:
Мышьякобензолы
Хлорамфеникол
Сульфамид
Стрептомицин
2. Противосудорожные:
Мезантоин
Триметадион
3. Антитиреоидные: Метилтиоурацил
4. Антигистаминные: Фенерган
5. Инсектициды: ДДТ
6. Различные факторы:
Соли золота
Фенилбутазон
Нитрофенол
Мепробамат
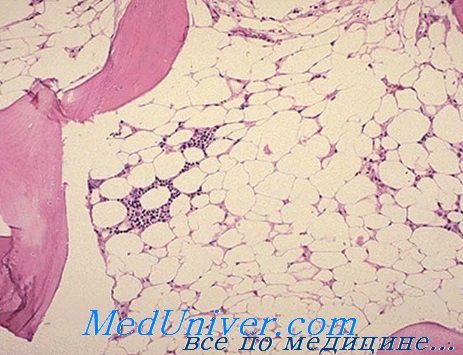
Бензол и его соединения как причина апластической анемии. Несчастные случаи, вызываемые бензолом, начали обнаруживаться в начале нашего века, в связи с промышленным применением этого вещества в качестве органического растворителя (Robr). В принципе бензол угнетает костный мозг, что означает приостановление синтеза РНК в уже дифференцированных элементах.
Видимо бензол не угнетает колонии клеток-штамм, в чем следует искать объяснение полной обратимости нарушений в случаях непродолжитекьности токсического воздействия (Nomiyama).
Влияние на костный мозг тесно связано с количеством воздействующего на больного вещества. Исходно отмечается раздражение костного мозга и общая, в частности эритроидная, гиперплазия, сопровождающаяся лейкоцитозом, нейтрофилией и отклонением влево в периферической крови; затем, постепенно, развивается костномозговая гипоплазия с обширными участками жирного преобразования, наличием редких миелоидных элементов, выраженной реакцией лимфатической или плазмоцитной ткани, а в отдельных случаях моноцитной реакцией, которую часто нелегко различить от лейкемического поцесса (Мунтяну).
После развития костномозговой гипоплазии имеются лишь немногие шансы на его восстановление. Вот почему внимание направлено на предупреждение заболевания путем ограничения концентрации бензола в атмосферном воздухе соответствующих заводов, максимально до 34 частей на 1 млн. и выявление первых признаков поражения костного мозга с помощью наблюдения за развитием эритроцитного макроцитоза у рабочих данных предприятий (Мунтяну).
Однако бензол оказывает и ряд других влияний на костный мозг, в том числе обусловливает: выраженную гиперплазию эритроидного ряда и приостановление деления (мегалобластоз), картину, называемую бензоловой эритропатией, имеющей большое сходство с острой эритемией; хронический миелосклероз с миелоидной метаплазией; гипоплазию лимфатической тнани, равно как и острую лейкемию (Rohr, Wintrobe).
Хлорамфеникол это антибиотик, вызвавший большой энтузиазм в 1948 г. когда был проверен его чрезвычайный эффект при заболеваниях брюшным тифом, а затем и отдельными риккетсиозами. Но в дальнейшем широкое применение препарата в борьбе с инфекцией грамм-отрицательными возбудителями начало выявлять его вредные последствия, поскольку он способствует развитию весьма тяжелой необратимой костномозговой аплазии.
В клинике риск развития аплазии после лечения хлорамфениколом составляет 1/10 тыс.—1/20 тыс. Однако по иным статистическим данным, например Объединения американских врачей, хлорамфеникол составил причину развития 44% всех заболеваний панцитопенией в США (Williams).
Формула хлорамфеникола включает бензоловое ядро с боковой цепью дихлорацетамида (Мунтяну). В связи с этим создалось мнение о том, что токсический эффект следует отнести за счет бензолового ядра. За справедливость такого предположения говорит и тот факт, что, подобно бензолу, медикамент поражает исходно эритроидный ряд, приостанавливая созревание, блокируя включение железа в гем с последующим ростом показателей сывороточного железа, костномозговых сидеробластов и развитием ретикулоцитопении.
Дальнейшие исследования выявили одновременное по существу поражение всех рядов крови, при этом первым морфологическим признаком поражения костного мозга оказалось появление вакуолей в костномозговых клетках, которые лучше выражены в эритробластах (Мунтяну, Ward).
Эти данные совпадают с результатами экспериментальных наблюдений, по которым медикамент угнетает синтез белков в клетках костного мозга в результате соревнования с ARNm (Ward), а также и синтез РНК (Williams).
В дальнейшем были обнаружены довольно тяжелые осложнения спустя некоторое время после прекращения лечения этим медикаментом. В связи с этим была выдвинута гипотеза о возможных, вызываемых им изменениях в геноме клеток-штамм, результатом чего являются необратимые сдвиги механизма деления последних, развитие необратимой костномозговой аплазии и острой лейкемии (Mukherji) или ночной пароксизмальной гемоглобинурии (Дачие и Левис).
В клинической практике целесообразно помнить, что этот медикамент вызывает тяжелые, смертельные аплазии и его применение следует ограничивать заболеваниями, вызываемыми строго чувствительными к нему возбудителями.
Прочие химические агенты, приводящие к апластической анемии. К категории иных химических факторов, обусловливающих костномозговую аплазию относятся ДДТ, сульфонамиды, противосудорожные средства, равно как и соединения золота. Также доказано, что атебрин создает чрезмерную чувствительность и тем самым способствует развитию костномозговой аплазии.
Ночная пароксизмальная гемоглобинурия как последствие апластической анемии. По результатам ряда наблюдений ночная пароксизмальная гемоглобинурия развивается после костномогзовой аплазии (Dacie и Lewis). Описаны также 2 случая костномозговой аплазии, сопровождающейся ночной пароксизмальной гемоглобинурией, а в конечном итоге — острой миелобластической лейкемией («трехзтапная» эволюция) (Holden и Lichtman).
Утверждается, что, по началу, токсический агент поражает (вызывает мутацию) клетки-штамм (Dacie и Lewis). Выживающие при этом клетки-штамм порождают аномальные популяции: эритроцитов — чувствительных к комплементу, гранулоцитов — лишенных лейкоцитной щелочной фосфатазы и тромбоцитов с недостатком ферментов.
Апластическая анемия отмечена и при беременности (Evans), гипопитуитаризме, почечной недостаточности и пр.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Апластическая анемия
Апластическая анемия – серьёзное нарушение формирования, развития и созревания клеток крови. Оно характеризуется угнетением кроветворной функции костного мозга, что проявляется дефицитом образования белых и красных кровяных клеток, а также тромбоцитов. Иногда наблюдается недостаток формирования только эритроцитов. Заболевание считается одним из самых тяжёлых расстройств гемопоэза и при отсутствии адекватного лечения может стать причиной летального исхода в течение нескольких месяцев. Оно в одинаковой степени поражает пациентов мужского и женского пола в возрасте от десяти до двадцати пяти лет или старше пятидесяти. Согласно медицинской статистике каждый год диагностируют два случая патологии на один миллион человек.
Пройти диагностику и лечение апластической анемии в Москве предлагает отделение гематологии ЦЭЛТ. Наша многопрофильная клиника одна из первых в РФ начала деятельность на рынке платных медицинских услуг и успешно продолжает её уже третье десятилетие. В отделении гематологии ведут приём ведущие отечественные специалисты, в арсенале которых имеется современная лечебно-диагностическая база, позволяющая точно ставить диагноз и проводить лечение в соответствии с международными стандартами. Стоимость услуг доступна в нашем прайс-листе, который мы регулярно обновляем. Во избежание недоразумений просим Вас уточнять цифры у операторов нашей информационной линии: +7 (495) 788 33 88.
Апластичная анемия: этиология
Согласно происхождению, выделяют врождённую и приобретённую анемию. Первая развивается вследствие хромосомных мутаций, вторая – под воздействием химических веществ, излучения, инфекций. Специалисты считают, что угнетение кроветворения костного мозга может быть инициировано появлением в нём и в крови цитотоксических Т-лимфоцитов. Они производят ФНО (внеклеточный белок) и интерферон “y”, которые подавляюще воздействуют на ростки кроветворения. Причина запуска механизма может крыться в:
- Воздействии ионизирующего излучения или химических веществ в виде ароматических соединений, мышьяка, пестицидов;
- Попадании в организм инфекционных агентов (возбудители гепатитов “D”, “B”, цитомегаловируса, ДНК-содержащего вируса Эпштейна-Барр);
- Приёме миелотоксических препаратов при прохождении курса лечения транквилизаторами, противосудорожными, антитиреоидными и антиопухолевыми средствами;
- Развитии ряда аутоиммунных процессов (красная системная волчанка, поражение соединительной ткани – синдром Шегрена).
В 50% случаев причину развития патологии установить не удаётся. Такая форма апластической анемии называется идиопатической.
Классификация апластической анемии
| Форма патологии | Чем отличается? |
| По продолжительности течения | |
| Острая | Не более одного месяца |
| Подострая | От одного месяца до полугода |
| Хроническая | Более полугода |
| По степени тяжести при избирательной аплазии | |
| Умеренная | Гранулоцитов менее 0,0х10 9 /л, тромбоцитов менее 20,0х10 9 /л. |
| Тяжёлая | Гранулоцитов менее 0,5х10 9 /л, тромбоцитов менее 20,0х10 9 /л. согласно результатам диагностики клеточность костного мозга составляет менее трети от нормы. |
| Очень тяжёлая | Гранулоцитов более 0,5х10 9 /л, тромбоцитов более 20,0х10 9 /л. |
Апластическая анемия: симптомы
Заболевание начинается остро, оно сопровождается ощущением сильной слабости и быстрой утомляемостью. Кожные покровы больного и видимые слизистые оболочки выглядят бледными, а сам он страдает от следующих клинических проявлений:
- шум в ушах;
- появление одышки даже при несущественных усилиях;
- неприятное покалывание в области грудной клетки.
При снижении количества тромбоцитов в единице объёма крови проявляется геморрагический синдром:
- даже после незначительной компрессии или ударах кожного покрова на нём появляются синяки и кровоизлияния;
- на теле, руках и ногах можно увидеть сыпь в виде мелких точек;
- наблюдается кровоточивость дёсен;
- спонтанные кровотечения из носа;
- обильные менструации (у женщин).
Снижение количества лейкоцитов в единице объёма крови характеризуется регулярным частым развитием инфекционных заболеваний кожи и структур мочевыводящей системы, воспалительными процессами слизистой оболочки рта, воспалениями лёгких.
Врождённая форма анемии развивается у детей до десяти лет и сопровождается целым рядом других нарушений:
- недоразвитие черепа и головного мозга;
- снижение размеров и массы почек (гипоплазия);
- интенсивная окраска отдельных участков кожи – гиперпигментация;
- сильное снижение слуха и нарушения речевой функции из-за него.
Апластическая анемия: осложнения
Отсутствие лечения апластической анемии может привести к летальному исходу из-за развития таких осложнений, как:
- инфекционные заболевания;
- кровоизлияние в головной мозг;
- анемическая кома;
- сильные кровотечения.
Апластическая анемия: диагностика
Перед тем, как приступить к лечению заболевания, гематологи ЦЭЛТ проводят комплексную диагностику, направленную на точную постановку диагноза и выявление этиологического фактора. Она включает в себя:
- осмотр у гематолога;
- общий и биохимический анализы крови;
- забор образца костного мозга и его исследование – стернальная пункция.
При наличии заболевания у пациента выявляют серьёзное снижение гемоглобина, вплоть до критического уровня – 20-30 г/л, наблюдается агранулоцитоз – снижение зернистых лейкоцитов и моноцитов. Количество лимфоцитов может быть в норме или сниженным, тромбоцитов – всегда снижено, иногда их не обнаруживают вовсе. Скорость оседания эритроцитов – повышается до 4-60 мм/ч. Исследование образца костного мозга выявляет повышенное содержание жировой ткани – 90%, включающее в себя элементы стромы и лимфы, а вот гематогенные клетки имеются в очень малом количестве.
Лечение апластической анемии
Лечение идиопатической и других видов апластической анемии – очень сложная задача, требующая комплексного индивидуального подхода. При разработке тактики специалисты ЦЭЛТ учитывают результаты диагностики и показания пациента. Больного помещают в изолятор с асептическими условиями, что позволяет исключить риск развития инфекций и их осложнений. Медикаментозная терапия заключается в приёме:
- Глюкокортикоидов – при выявлении аутоиммунных механизмов и формировании антител против собственных кровяных клеток;
- Цитостатиков – при отсутствии эффекта от лечения глюкокортикоидами при аутоиммунной анемиии;
- Циклоспорина «А» – для подавления производства ФНО и интерферона “y”;
- Анаболиков – для стимулирования функции кроветворения;
- Андрогенов – для стимулирования образования красных кровяных клеток.
Всем больным апластической анемией проводят переливание эритроцитарной и/или тромбоцитарной массы, в объёмах, определяемых исходя из клинической картины и показателей периферической крови. Кроме того, пациенту могут назначить спленэктомию – хирургическое вмешательство, направленное на удаление селезёнки. Самые благоприятные прогнозы может обеспечить трансплантация костного мозга. Она заключается в пересадке донорских или собственных стволовых кроветворных клеток, предварительно изъятых из подвздошных костей путём пункции. К сожалению, процедура недоступна для широкого применения из-за сложности подбора совместимого донора. В том случае, если это невозможно, пациенту назначают паллиативную терапию с применение циклоспорина А.
В отделении гематологии нашей клиники ведут приём кандидаты, доктора и профессоры медицинских наук с опытом практической и научной работы от двадцати пяти лет. Вы можете записаться к ним на приём онлайн или обратившись к нашим операторам. Специалисты высокой квалификации работают и в отделении урологии. К ним можно записаться на цистоскопию мочевого пузыря.
Записавшись на прием гематолога, вы сможете получить всестороннюю консультацию. В компетенции врача находится лечение различных заболеваний крови, большинство из которых можно выявить на ранних стадиях и назначить своевременное лечение, позволяющее справиться с болезнью быстро и легко.
Апластическая анемия ( Гипопластическая анемия )
Апластическая анемия – угнетение функции кроветворения красного костного мозга (эритроцитопоэза, лейкопоэза и тромбоцитопоэза), приводящее к пангемоцитопении. К основным клиническим проявлениям гематологического синдрома принадлежат головокружение, слабость, обмороки, одышка, покалывание в груди, кожные геморрагии, кровотечения, склонность к развитию инфекционно-воспалительных и гнойных процессов. Заболевание диагностируется на основании характерных изменений гемограммы, миелограммы и гистологического исследования трепанобиоптата. Лечение патологии включает проведение гемотрансфузий, иммуносупрессивной терапии, миелотрансплантации.
МКБ-10



Общие сведения
Апластическая (гипопластическая) анемия – тяжелое расстройство гемопоэза (чаще всех его звеньев), сопровождающееся развитием анемического, геморрагического синдромов и инфекционных осложнений. Развивается в среднем у 2 человек на 1 млн. населения в год. Приблизительно с одинаковой частотой патология поражает мужчин и женщин. Возрастные пики заболеваемости приходятся на возраст 10–25 и старше 50 лет. При данной патологии в костном мозге чаще нарушается образование всех трех типов клеточных элементов крови (эритроцитов, лейкоцитов и тромбоцитов), иногда — только одних эритроцитов; в зависимости от этого различают истинную и парциальную апластическую анемию. В гематологии данный вид анемии относится к числу потенциально фатальных заболеваний, приводящих к гибели 2/3 заболевших.

Причины
По происхождению апластическая анемия может быть врожденной (связанной с хромосомными аберрациями) и приобретенной (развившейся в течение жизни). Принято считать, что угнетение миелопоэза связано с появлением в красном костном мозге и крови цитотоксических T-лимфоцитов, производящих фактор некроза опухолей и γ-интерферон, которые в свою очередь подавляют ростки кроветворения. Запускать этот механизм могут различные внешнесредовые (химические соединения, физические явления, лекарственные вещества), а также эндогенные факторы (вирусы, аутоиммунные реакции). К числу наиболее значимых причин относят:
- Прием миелотоксических препаратов. Достоверно установлена связь анемии с приемом некоторых противоопухолевых, противосудорожных, антибактериальных, антитиреоидных, противомалярийных препаратов, транквилизаторов, препаратов золота и др., обладающих потенциальным миелотоксическим эффектом. Лекарственные вещества могут вызывать как прямое повреждение стволовых кроветворных клеток, так и опосредованное — через аутоиммунные реакции. Анемии, связанные с таким механизмом развития, называются лекарственными.
- Контакт с химическими и физическими агентами. Супрессию костного мозга может вызывать взаимодействие с органическими растворителями, соединениями мышьяка, бензольными соединениями, пестицидами, облучение всего тела. В некоторых случаях недостаточность гемопоэза является временной и обратимой — главными факторами здесь являются концентрация/доза вещества и время контакта. супрессию костного мозга.
- Вирусные инфекции. Из вирусных агентов наибольшее значение уделяется возбудителям гепатитов В, С и D. В этом случае гипопластическая анемия обычно развивается в течение полугода после перенесенного вирусного гепатита. При изучении патогенеза было замечено, что репликация вируса происходит в мононуклеарах крови и костного мозга, а также в иммунных клетках. Предполагается, что подавление миелопоэза в этом случае является своеобразным иммунным ответом, возникающим против клеток, несущих на своей поверхности вирусные антигены. Такой вид анемии выделяется в отдельную форму – постгепатитную. Среди других вирусных инфекций называются ЦМВ, инфекционный мононуклеоз, грипп.
Также описаны случаи панцитопении, вызванные инфицированием туберкулезом, интоксикацией, лучевой болезнью, лимфопролиферативными заболеваниями (тимомой, лимфомой, хроническим лимфобластным лейкозом), беременностью. Почти в половине наблюдений причину анемии выявить не удается — такие случаи относят к идиопатической форме.
Патогенез
В основе апластической анемии может лежать либо первичное повреждение гемопоэтических стволовых клеток, либо нарушение их эффективной дифференцировки. При наследственных анемиях недостаточность гемопоэза опосредована кариотипическими аберрациями, приводящими к нарушению репарации ДНК и невозможности репликации стволовых клеток костного мозга. В случае приобретенной анемии под влиянием этиофакторов наблюдается активация Т-клеток, которые начинают продуцировать цитокины (интерферон-гамма, ФНО), поражающие клетки-предшественники гемопоэза. В стволовых клетках костного мозга повышается экспрессия генов, отвечающих за апоптоз и активизацию клеточной гибели. Основные клинические проявления обусловлены пангемоцитопенией – снижением в составе крови всех ее форменных элементов (эритроцитов, лейкоцитов, тромбоцитов).
Классификация
Кроме различных этиологических вариантов (лекарственного, постгепатитного, идиопатического), различают острую (до 1 мес. течения), подострую (от 1 до 6 мес.) и хроническую (более 6 мес.) форму заболевания. Анемию, протекающую с избирательным угнетением эритропоэза, называют парциальной красноклеточной аплазией. На основании выраженности тромбо- и гранулоцитопении данная форма анемии подразделяется на 3 степени тяжести:
- очень тяжелую (тромбоцитов менее 20,0х109/л; гранулоцитов менее 0,2х109/л)
- тяжелую (тромбоцитов менее 20,0х109/л; гранулоцитов менее 0,5х109/л), по данным трепанобиопсии – низкая клеточность костного мозга (менее 30% от нормы)
- умеренную (тромбоцитов более 20,0х109/л; гранулоцитов более 0,5х109/л)
Симптомы апластической анемии
Поражение трех гемопоэтических ростков (эритро-, тромбоцито- и лейкопоэза) обусловливает развитие анемического и геморрагического синдромов, инфекционных осложнений. Дебют апластической анемии обычно происходит остро. Анемический синдром сопровождается общей слабостью и утомляемостью, бледностью кожи и видимых слизистых, шумом в ушах, головокружением, покалыванием в груди, одышкой при нагрузке.
Основным проявлением тромбоцитопении выступает геморрагический синдром. Больные отмечают появление петехий и экхимозов на коже, повышенную кровоточивость десен, спонтанные носовые кровотечения, меноррагии. Возможно возникновение гематурии, маточных и желудочно-кишечных кровотечений. Следствием лейкопении и агранулоцитоза служит частое развитие инфекционных процессов – стоматитов, пневмоний, инфекций кожи и мочевыводящих путей. Для апластической анемий нехарактерны похудание, лимфаденопатия, гепато- и спленомегалия – при этих признаках следует искать другую причину пангемоцитопении.
Врожденная апластическая анемия (синдром Фанкони) обычно развивается у детей в возрасте до 10 лет и кроме аплазии костного мозга характеризуется другими нарушениями: микроцефалией, гипоплазией почек, низкорослостью, аномалиями развития верхних конечностей (гипоплазией первой пястной и лучевой кости), гипоспадией, гиперпигментацией кожи, крайней степенью тугоухости и др. При наследственной анемии Эстрена-Дамешека отмечается тотальное поражение кроветворения и панцитопения при отсутствии врожденных аномалий развития. Для анемии Даймонда-Блекфена или парциальной красноклеточной аплазии характерно только снижение количества эритроцитов.

Осложнения
Летальный исход может быть обусловлен кровоизлияниями во внутренние органы, массивными кровотечениями, инфекционными осложнениями, анемической комой. Наиболее грозное из геморрагических осложнений – кровоизлияние в головной мозг (геморрагический инсульт). Больные склонны к частым и тяжело протекающим вирусным и бактериальным инфекциям респираторного тракта. Значительное или стремительное снижение уровня красных кровяных телец может привести к анемической коме. При молниеносной форме крайне быстро развиваются тяжелейшая анемия, иммунодефицит, коагулопатии, имеющие фатальные последствия.
Диагностика
Оценка гематологического статуса включает внимательный клинический осмотр и проведение тщательной лабораторной диагностики. При физикальном обследовании выявляется выраженная бледность или желтушность кожи, артериальная гипотония, тахикардия. Основу диагностического алгоритма составляет проведение общего и биохимического анализа крови, стернальной пункции, трепанобиопсии:
- Исследования крови. Для гемограммы при гипопластической анемии типичны эритро-, лейкоцито- и тромбоцитопения, нейтропения и относительный лимфоцитоз. Оценка биохимических показателей (печеночных проб, нефрологического комплекса, сывороточного железа, билирубина) информативна для исключения других анемий.
- Исследованиепунктата костного мозга. В миелограмме обнаруживается уменьшение количества миелокариоцитов и мегакариоцитов, снижение клеточности. В трепанобиоптате определяется замещение красного костного мозга жировым (желтым).
В рамках диагностического поиска апластическую анемию необходимо дифференцировать с мегабластными (В12-дефицитными, фолиеводефицитными) анемиями, идиопатической тромбоцитопенической пурпурой, пароксизмальной ночной гемоглобинурией, острым лейкозом.

Лечение апластической анемии
Больные с апластической анемией госпитализируются в специализированные отделения. Им обеспечиваются полная изоляция и асептические условия для предупреждения возможных инфекционных осложнений. Проведение эффективного лечения является сложной проблемой практической гематологии. В зависимости от уровня цитопении используются следующие лечебные подходы:
- Иммуносупрессиная терапия. При умеренной цитопении назначается фармакотерапия, включающая комбинацию антитимоцитарного иммуноглобулина и циклоспорина А. Поддерживающая терапия проводится анаболическими стероидами или их сочетанием с циклоспоринами.
- Гемотрансфузии. В комплексе с курсом иммуносупрессивной терапии при низких показателях красной крови показано проведение заместительной гемотрансфузионной терапии (переливание тромбоцитов и эритроцитарной массы), плазмафереза. Данная мера не оказывает воздействия на патогенетическое звено заболевания, но позволяет восполнить дефицит кровяных телец, не вырабатываемых костным мозгом.
- Трансплантация КМ и СК. Наиболее благоприятные прогнозы на долгосрочную выживаемость оказывает выполнение аллогенной трансплантации костного мозга. Однако ввиду сложности подбора иммунологически совместимого донора процедура используется ограниченно. В качестве экспериментальных подходов рассматриваются аутологичные трансплантации, пересадка стволовых клеток периферической крови. Больным с нетяжелой формой анемии может быть показано проведение спленэктомии, эндоваскулярной окклюзии селезеночной артерии.
Прогноз и профилактика
Прогноз определяется этиологической формой, тяжестью и остротой течения анемии. Критериями неблагоприятного исхода служат быстрое прогрессирование заболевания, тяжелый геморрагический синдром и инфекционные осложнения. После трансплантации костного мозга ремиссии удается достичь у 75–90% пациентов. Первичная профилактика данной разновидности анемии предполагает исключение влияния неблагоприятных внешнесредовых факторов, необоснованного применения лекарственных препаратов, предупреждение инфекционной заболеваемости и др. Пациентам с уже развившимся заболеванием требуется диспансерное наблюдение гематолога, систематическое обследование и длительная поддерживающая терапия.
2. Комплексная программа диагностики апластической анемии с определением прогностически значимых патогенетических особенностей заболевания. Методические рекомендации. — 2015.
4. Апластическая анемия: современные представления о патогенезе и терапии/ Айсариева Б. К., Раймжанов А. Р., Айтбаев К.// Молодой ученый. — 2011 — №9.
Апластическая анемия
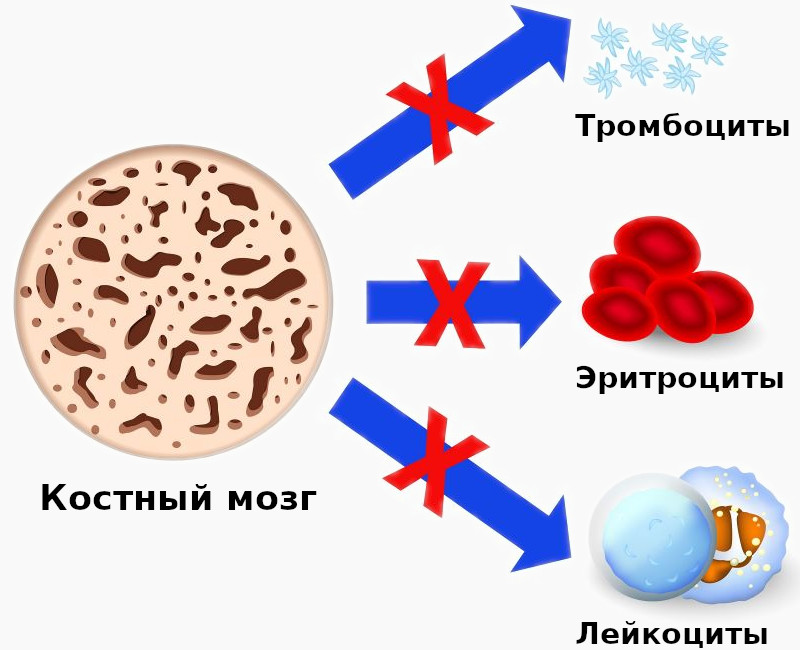
Апластическая анемия — это заболевание, которое характеризуется периферической панцитопенией. То есть, это такое состояние при котором костный мозг человека перестает производить достаточное количество клеток крови.
При апластической анемии возникает дефицит всех типов клеток: эритроцитов, лейкоцитов и тромбоцитов.
Костный мозг — это своеобразная структура, которая находится в костном канале. Он отвечает за образование всех клеток крови, для того чтобы снабжать организм кислородом, бороться с инфекцией и обеспечивать свертываемость крови. И если в его работе возникают сбои, или клетки костного мозга повреждаются различными факторами, они перестают производить новые кровяные клетки и развивается апластическая анемия.
Чаще всего развивается в молодом и детском возрасте, от 10 до 20 лет. Но иногда отмечается еще один пик развития болезни в 60 лет. Распространенность между мужчинами и женщинами примерно одинакова.
Впервые апластическую анемию описал немецкий ученый врач Поль Эрлих, в 1888 году. Он проводил исследования причины смерти беременной женщины, молодого возраста, что достаточно скоропостижно умерла. На вскрытии, врач увидел, что во внутрикожном пространстве, нормальная ткань отсутствует. Она была замещена жировой. Тогда он и предположил, что это одно из самых тяжелых заболеваний гемопоэза. Правда, термин “апластическая анемия”был применен только в 1904 году, французским гематологом А. М. Шоффаром
Этиология апластической анемии
Чаще всего, это приобретенное заболевание, которое возникает в течение жизни, а не передается по наследству.
Точную причину развития апластической анемии найти достаточно сложно, так как в повседневной жизни мы сталкиваемся с многими факторами, которые могут влиять на работу костного мозга.
Ученые выделяют основные триггеры, что могут стать пусковым механизмом:
* Воздействие различных химикатов. Некоторые вещества, что используются в пестицидах, бензол, хлоры, нитраты, могут повреждать костный мозг.
* Различные излучения. Радиационные, магнитные и прочее плохо влияет на работу всего организма и может привести к тому, что и костный мозг не сможет справиться с нагрузкой.
* Наличие вирусных заболеваний. Около 2% больных на вирусный гепатит, страдают от апластической анемии. Также сюда относят цитомегаловирус, ВИЧ, Эпштейн-Барр и парвовирусы. https://www.nejm.org/doi/full/10.1056/nejm199705083361906
* Фармакологические препараты и некоторые методы лечения. Например, некоторые сильные антибиотики, химиопрепараты и радиационная терапия.
* Аутоиммунные заболевания. Это патологическое состояние, когда собственная иммунная система начинает атаковать клетки своего организма. В большинстве случаев, страдает и костный мозг
Одним из факторов риска развития, является отягощенный наследственный анамнез. Собственно, если в семье были случаи апластической анемии, то под действием триггеров, она может развиваться.
Симптоматика апластической анемии
Конкретных, специфических симптомов у апластической анемии нет. Врачи оценивают все жалобы в комплексе и только потом могут заподозрить болезнь.
Так как при апластической анемии отсутствует полноценное количество всех клеток крови, то и симптомы проявляются в результате невыполнения их функций.
Отсутствие эритроцитов приводит к тому, что организм не получает необходимые микроэлементы, и что более важно — кислорода. Это приведет к:
— Постоянной слабости, усталости и потери трудоспособности;
— Головной боли и головокружению;
Потеря лейкоцитов приведет к снижению иммунной защиты, а значит может проявляться:
— Частыми инфекционными заболеваниями;
А при уменьшении количества тромбоцитов теряется функция свертываемости крови, и симптомами этого будет:
— Появления синяков, даже при малейшем физическом воздействии;
— Наличие красной сыпи по телу;
— Длительное кровотечение из небольших ран, что трудно остановить;
— Кровоподтеки с десен во время чистки зубов или приема пищи.
Болезнь может развиваться довольно долго. Гемопоэз не отключается полностью, его функция снижается постепенно. И по началу, пациент не чувствует никаких симптомов, так как организм компенсирует и работает нормально, хоть и с меньшим количеством клеток. Но со временем, запасы и депо клеток истощаются, а костный мозг продолжает терять свою функцию и тогда симптомы начинают нарастать. Иногда, люди не понимают что именно происходит и занимаются домашним самолечением, что только приводит к усугублению состояния. А при критически низком уровни клеток, возникают неотложные состояния.
Диагностические мероприятия
Диагностика апластической анемии не такая уж и сложная. Большинство случаев находят во время профилактических осмотров. Достаточно сдачи одного общего анализа крови, чтобы заподозрить наличие апластической анемии.
Тогда врач начинает детальный сбор жалоб пациента, анамнез, отмечает характерные для апластической анемии симптомы.
И тогда уже врач назначает более детальные исследования для точной постановки диагноза, определения степени сложности.
Так при подозрении на АА врач назначает аспирацию костного мозга. Далее костный мозг осматривают под микроскопом, оценивают наличие и состояние клеток крови еще на стадии их развития. При апластической анемии костный мозг обеднен всеми клеточными ростками. Основным диагностическим методом при АА является трепанобиопсия костного мозга, которая позволяет наиболее точно оценить состояние кроветворения.
Также Врач назначает:
— Серологические исследования на гепатит и другие вирусные образования;
— Лабораторные анализы для исследования функции почек и печени;
— Ультразвуковую диагностику. Прицельно могут осматривать увеличенные лимфоузлы.
— Анализ на антитела к инфекциям;
Иногда необходимо пройти и другие исследования для уточнения диагноза и установления причины развития апластической анемии.
Хотя, довольно часто, причина остается неизвестной, из-за большого количества факторов и триггеров, что могут спровоцировать ее.
Лечение апластической анемии
После всех исследований врач определяет курс терапии. Если во время диагностики все таки удалось установить причину развития, то в первую очередь необходимо избавиться от триггера, который повреждает стволовые клетки костного мозга.
Для полноценного лечения апластической анемии необходимы комплексный подход, то есть применение фармакологии и специфических манипуляций.
Пересадка костного мозга.
Трансплантация стволовых клеток для восстановления костного мозга стволовыми клетками от донора может быть единственным успешным вариантом лечения для людей с тяжелой апластической анемией.
Методами лечения АА считаются иммуносупрессивная терапия и аллогенная пересадка костного мозга. Чаще всего используют родственного донора (брата или сестру) или ищут в специальных базах доноров. После процедуры реципиент находится под наблюдением врачей. Когда стволовые клетки начнут работать и запустят гемопоэз, врачи отпускают больного домой.
Конечно, для реципиента эта процедура достаточно опасна, так как организм может не принять трансплантат, а собственных клеток не будет. Поэтому, для избежания такого состояния, пациенту выписываются препараты, который помогут предотвратить отторжение.
Стоит учитывать, что при использовании родственных доноров(братьев или сестер), показатель успешности вырастет, чем неродственных.
К фармакологическим методам лечения относится применение:
- Иммунодепрессантов. Это препараты, которые подавляют иммунную систему пациента. применяется когда у пациента с тяжелой формой АА нет родственного донора. Таким образом, иммунная система перестает атаковать костный мозг, он может восстановиться и начать создавать здоровые клетки.
Для этого используют такие препараты:
Также дополнительно назначаются кортикостероиды.
2 Иногда в качестве симптоматической терапии используются стимуляторы костного мозга. Эти препараты помогают организму заставить костный мозг генерировать новые клетки. К ним относят филграстим, пэгфилграстим и другие.
- Дополнительные медикаменты. Так как апластическая анемия может сопровождаться большим количеством других заболеваний, которые возникли на фоне отсутствия клеток крови, то для полноценной терапии используют:
— Антибиотики или противовирусные. Для подавления бактерий и вирусов, которые атакуют организм из-за отсутствия лейкоцитов;
— Противовоспалительные. Для утоления головной боли, снятия жара.
— Противотошнотные. Их применяют, когда проводят пересадку костного мозга.
Переливание компонентов крови
Иногда апластическая анемия приводит к тому, что дефицит клеток крови настолько большой, что может угрожать жизни пациенту. Это может быть кровотечение, что не останавливается, тяжелая анемия. В таком случае врачи назначают переливание компонентов крови:
Одним из плюсов переливания крови, считается скорость действия, ведь эффект виден уже через несколько часов и почти неограниченное количество. Но существует большой риск развития осложнений от большого количества чужеродной крови. А также, переливание крови не считается методом лечения апластической анемии. Это исключительно симптоматическое лечение, которое требует немедленного восстановления количества клеток.
Своевременное и современное лечения с помощью медикаментов и пересадки костного мозга апластической анемии повышает выживаемость на протяжении пяти лет, в 42%. При этом, в молодом возрасте, этот показатель в разы больше, чем в старшем.
Апластическая анемия

Разработчик сайтов, журналист, редактор, дизайнер, программист, копирайтер. Стаж работы — 25 лет. Область интересов: новейшие технологии в медицине, медицинский web-контент, профессиональное фото, видео, web-дизайн. Цели: максимально амбициозные.
- Запись опубликована: 01.09.2020
- Reading time: 5 минут чтения
Апластическая анемия — это заболевание крови, форма анемии, при которой в костном мозге недостаточно тромбоцитов (эритроцитов), эритроцитов и лейкоцитов. Это редкое заболевание, которое может возникнуть в любом возрасте. Болезнь может развиваться медленно или быстро.
Что такое апластическая анемия
Апластическая анемия — это патологическое состояние организма, при котором костный мозг перестает вырабатывать все три типа клеток крови: красные кровяные тельца (эритроциты), белые кровяные тельца (лейкоциты) и тромбоциты (тромбоциты). Это происходит, когда по какой-то причине в костном мозге уменьшается количество стволовых клеток, из которых развиваются все клетки крови.
Точнее сказать — это синдром недостаточности костного мозга, характеризующийся снижением количества эритроцитов, лейкоцитов, тромбоцитов в крови и гипоплазией костного мозга с менее чем 30% гематопоэтических клеток.

Что такое апластическая анемия
Апластическая анемия подразделяется на первичную и вторичную.
- Первичная — анемия Фанкони, врожденный склероз и семейная апластическая анемия.
- Вторичная — анемия, вызванная химическими веществами, лекарствами, вирусами.
Распространенность
Апластическая анемия — относительно редкое заболевание: заболеваемость составляет 5-10 случаев на миллион людей в год.
Симптомы апластической анемии
Больные жалуются на нарастающую слабость, утомляемость, нехватку воздуха. Возможно кровотечение, быстрее возникают синяки. У пациентов с анапластической анемией более частые инфекции, высокая температура с ознобом — серьезное состояние, требующее безотлагательного медицинского обследования и лечения.
Часто встречающиеся симптомы:
- общая слабость;
- быстрая утомляемость;
- одышка в покое и во время упражнений;
- частое сердцебиение;
- аритмичное сердцебиение;
- бледная кожа;
- кровотечение из ран;
- синяки на коже;
- кровотечение из носа ;
- десневое кровотечение;
- общие инфекции;
- высокая температура ;
- головная боль.


Этиология. Причины развития апластической анемии
Апластическая анемия возникает при повреждении костного мозга, который производит стволовые клетки крови. Производство клеток может замедляться, они могут полностью разрушаться или производиться в деформированном, дисфункциональном виде. В 65% случаях причина заболевания неясна.
Врожденные патологии . Врожденная апластическая анемия встречается редко. Наиболее частой формой врожденного заболевания является синдром Фанкони: пациенты с низким ростом, измененной пигментацией кожи, различными проблемами с почками. Генетическое тестирование в этом случае выявляет хромосомные аберрации.
Лекарства и токсины. Наиболее частой известной причиной апластической анемии является воздействие лекарств и токсинов окружающей среды.

Причина апластической анемии – воздействие лекарств
Недостаточность костного мозга, наряду с апластической анемией, часто вызвана токсинами — органическими химикатами (бензолом, толуолом, инсектицидами, нефтяными дистиллятами).
Что касается лекарств, апластическая анемия вызывается:
- антибиотиком хлорамфениколом;
- пеницилламином — используется для лечения заболеваний суставов;
- карбамазепином и фенитоином — используется для лечения эпилепсии;
- ацетазоламидом — диуретик;
- цитотоксическими препаратами, используемыми для лечения рака.
Встречаются случаи апластической анемии, развивающиеся на фоне вирусных инфекций — парвовирус B19, вирусы гепатита B и C, вирусы Эпштейна-Бар (EBV), цитомегаловирусы (CMV). Очень редко апластическая анемия возникает при беременности.
Цитотоксические препараты подавляют и убивают клетки костного мозга, но костный мозг восстанавливается довольно быстро, после прекращения их приема. Угнетает костный мозг и лучевая терапия. Иногда химиотерапией намеренно разрушают костный мозг при подготовке к трансплантации.
Течение болезни
Заболевание может развиваться очень медленно, а может возникать очень внезапно. Обычно апластическая анемия развивается незаметно и подозревается при возникновении комплекса различных симптомов. В некоторых случаях, например, при лечении рака, апластическая анемия довольно распространена и считается осложнением, в других случаях диагноз может быть отложен.
У пациента отсутствуют все клетки крови, что вызывает множество сопутствующих симптомов.
- Недостаток эритроцитов характеризуется одышкой, слабостью, утомляемостью, бледностью, головной болью, шумом в у шах.
- Недостаток тромбоцитов приводит к длительному кровотечению во время травмы или менструации, появлению синяков даже от малейших травм, покраснению глаз, спонтанному кровотечению из носа и десен.
- Отсутствие лейкоцитов характерно для частых инфекций, более трудно заживающих ран, лихорадки, иногда с ознобом.
Диагностика апластической анемии
Диагноз ставится на основании физического обследования — увеличение печени, возможные аномалии развития, изменение пигментации, быстрый рост, высокое небо, клинических симптомов, лабораторных тестов.
Важные клинические симптомы включают слабость, одышку (указывающую на возможное уменьшение количества эритроцитов), лихорадку, озноб, боль в горле (указывающую на возможную инфекцию из-за уменьшения лейкоцитов), кровотечения или синяки в различных частях тела, петехии (небольшие кровотечения) в слизистой оболочке рта (из-за уменьшения тромбоцитов). Пациент может быть бледным и иметь язвы во рту.
При осмотре глазного дна часто наблюдаются кровоизлияния в сетчатку.
При обследовании важно определить показатели крови , оценить степень истощения костного мозга и, если возможно, найти причину.
- Выявляется уменьшение количества всех клеток крови (эритроцитов (эритроцитопения), лейкоцитов (лейкоцитопения), тромбоцитов (тромбоцитопения)) – тогда состояние называется панцитопенией.
- Уменьшение количества нейтрофилов указывает на тяжесть апластической анемии: 0,5 х 10 9/ л показывают тяжелую и 0,2 х 10 9 / л – очень тяжелую апластическую анемию.
В случае заметного уменьшения количества кровяных телец требуется срочная консультация гематолога. Чтобы поставить диагноз, он выполняет аспирацию костного мозга или биопсию трепана, при которой из костного мозга берется небольшое количество клеток для более точного исследования. Это исследование помогает отличить апластическую анемию от других заболеваний крови.


Также проводится УЗИ внутренних органов. При необходимости цитогенетические исследования.
Лечение
Если возможно, следует устранить причину недостаточности костного мозга и апластической анемии. Иногда функция костного мозга восстанавливается, когда причина легкая, при только симптоматическом лечении легкой апластической анемии. Если количество клеток не очень велико, достаточно наладить питьевой режим и перейти на специальную диету.
Тяжелые и очень тяжелые формы апластической анемии представляют собой опасные для жизни состояния, требующие срочного и серьезного лечения. При температуре выше 38 o C в течение более двух часов пациента госпитализируют и лечат антибиотиками.

Лечение апластической анемии антибиотиками
Может потребоваться дополнительная инфузия тромбоцитов, когда риск кровотечения становится высоким — количество тромбоцитов падает ниже 10 x 10 9/ л. Инфузия эритроцитов назначается при тяжелых симптомах анемии.
Трансплантация костного мозга является методом выбора для лечения пациентов с тяжелой и очень тяжелой апластической анемией в возрасте до 50 лет. Пациенты старше 50 лет получают иммуносупрессивную терапию антитимоцитарным глобулином и циклоспорином.
В случае разрушения костного мозга из-за аутоиммунного процесса и невозможности трансплантации нельзя использовать иммунодепрессанты — циклоспорин, антитимоцитарный глобулин, метилпреднизолон, подавляющие атаку организма на костный мозг. Назначаются стимуляторы костного мозга — филрастин, колониестимулирующий фактор, эритропоэтин, др. Это препараты, стимулирующие костный мозг производить более специфические клетки. Лечение этими препаратами часто сочетается с иммуносупрессивной терапией.
В профилактических целях могут быть назначены антибиотики для предотвращения инфекций, поскольку сопротивляемость организма резко снижается.
В случае апластической анемии, вызванной лучевой терапией или химиотерапией для лечения рака, функция костного мозга восстанавливается после прекращения лечения.
Беременным женщинам делают переливание крови, и функция костного мозга также восстанавливается после родов, но если этого не происходит, лечение жизненно необходимо.
Осложнения
При тяжелой и очень тяжелой апластической анемии восприимчивость к различным инфекциям значительно увеличивается, и из-за низкого количества тромбоцитов возможно кровотечение. После трансплантации может возникнуть такая реакция отторжения, как сыпь, диарея, проблемы с печенью. Высокие дозы циклоспорина могут повышать артериальное давление, что приводит к почечной недостаточности.
Что такое супрессия костного мозга
Апластическая анемия — это болезнь, при которой повреждаются ростки в костном мозге, продуцирующие кровяные клетки. Это приводит к глубокому нарушению кроветворения и дефициту в организме основных кровяных клеток — эритроцитов, лейкоцитов и тромбоцитов. А поскольку каждая группа клеток выполняет свои функции, больной испытывает анемию (эритроциты), нарушение свертываемости крови (тромбоциты) и ослабление иммунитета (лейкоциты). В некоторых случаях страдает один росток — эритроцитарный, в других — все три ростка.
Впервые такая анемия описана еще в конце XIX столетия, но как отдельную болезнь ее зарегистрировали лишь в 1904 году. На миллион населения приходится от 2 до 5 случаев болезни, это редко, но летальность при апластической анемии доходит до 80%. Болеют главным образом дети и молодежь.
Причины: лекарства, вирусы, пестициды
Апластическая анемия бывает врожденной и приобретенной. Врожденная возникает вследствие мутаций соответствующих генов. На развитие приобретенной апластической анемии могут влиять множество различных факторов, включая прием некоторых лекарств, воздействие химических соединений (например, пестицидов), вирусов (в первую очередь вирусов гепатитов, но также цитомегаловирусов, гриппа, вируса Эпштейн—Барра), аутоантител, радиации (например, при работе в рентген-кабинете, лучевой терапии).
Среди лекарств, способных вызвать апластическую анемию — ряд антибиотиков, противосудорожные средства, средства для лечения малярии, препараты золота, препаратов для химиотерапии. По мнению гематологов, риск апластической анемии возрастает на фоне беременности, но как объяснить это явление, пока неизвестно. Первые же симптомы апластической анемии у беременной служат показанием к прерыванию беременности, в результате чего возможно наступлении ремиссии заболевания.
Признаки анемии

Клиническая картина апластической анемии складывается из признаков недостаточности эритроцитов, тромбоцитов и лейкоцитов. В случае эритроцитов на первый план выходят признаки анемии — слабость, вялость, бледность, покалывание в грудной клетке, снижение работоспособности, одышка, головокружение, приступы тахикардии, шум в ушах. Это так называемый анемический синдром.
Признаки снижения тромбоцитов: кровотечения
Геморрагический синдром обусловлен недостатком тромбоцитов. Он проявляется кровоподтеками на коже в отсутствии травм, петехиальной сыпью, частыми кровотечениями из носа, кровоточивостью десен, маточными и желудочно-кишечными кровотечениями. При тяжелом угнетении тромбоцитарного ростка возможен геморрагический инсульт.
Признаки снижения лейкоцитов: иммунитет

Признаком снижения количества лейкоцитов служит снижение иммунитета и, следовательно, высокая восприимчивость к разного рода инфекциям. За год у таких больных может отмечаться до 10 инфекционных заболеваний, причем многие из них протекают тяжело, с осложнениями. Так, если обычный человек переболеет ангиной и выздоровеет, то у больного апластической анемией разовьется язвенно-некротическая ангина, порез выльется в панариций, возможны пневмония, стоматиты, инфекции мочевыводящих путей, генерализованная форма сепсиса. Гепатомегалия (увеличение печени) и отеки ног говорят о сердечной недостаточности, однако размеры селезенки не изменяются, что является ценным критерием в диагностике.
Врожденные анемии
Следует также упомянуть о врожденной апластической анемии, или анемии Фанкони. Для нее, помимо нарушений кроветворения, характерны микроцефалия, недоразвитие почек, низкий рост, пороки развития верхних конечностей, потемнение кожи, нарушение слуха и другие симптомы. Анемия Эстрена-Дамешека характеризуется отсутствием других патологий, кроме угнетения продукции кровяных клеток. При анемии Даймонда-Блекфена страдает только эритроцитарный росток, а значит, отмечаются признаки анемии.
Диагностика и лечение апластической анемии

Общий осмотр больного выявляет наличие признаков анемии. В целях диагностики, кроме общего и биохимического анализов крови, берут образец костного мозга из грудины или подвздошной кости. Если известна причина анемии, естественно, первым шагом будет ее устранения. В основе терапии апластической анемии лежит заменное переливание крови, введение препаратов, стимулирующих кроветворение и пересадка костного мозга. Многократное переливание крови доноров ведет к накоплению в организме больного излишка железа. Поскольку скопление железа повреждает органы, назначают препараты, которые выводят железо. Переливание крови не делают в двух случаях: при аутоиммунной апластической анемии (это неэффективно) и перед пересадкой костного мозга — чтобы не произошло отторжение трансплантата.
Трансплантация костного мозга
При пересадке, или трансплантации, костного мозга роль донора может сыграть ближайший родственник. Перед процедурой больного подвергают лучевой и химиотерапии, а у донора берут кровь, фильтруют из нее стволовые клетки и вводят их больному. Так они попадают внутрь костей, где и начинается нормальное кроветворение. После процедуры больному назначают препараты против отторжения, которое, увы, все же иногда случается. После трансплантации ремиссия наступает в 75—90% случаев.
Другие методы лечения и прогноз

При аутоиммунной апластической анемии показаны иммунодепрессанты, которые дают тяжелые побочные эффекты, включая анафилактический шок, инфекции. Для предотвращения таких реакций назначают глюкокортикоиды.
В дополнение к проводимой терапии больным вводят так называемые колониестимулирующие факторы — лекарства, усиливающие продукцию костным мозгом лейкоцитов. Лечение длится две недели. Ограничением этого метода является высокая цена.
В работах ученых показано, что апластическая анемия эффективно лечится андрогенами. Назначают их только мужчинам на длительный срок. Кроме того, применяют удаление селезенки, в которой накапливаются кровяные клетки. Эта операция эффективна у 85% больных, в частности, после нее сразу уменьшается выработка аутоантител, направленных против своего костного мозга.
Прогноз апластической анемии определяется тяжестью течения последней и степенью снижения числа клеток крови. При тяжелой форме заболевания сохраняется высокая смертность. Но с введением в практику пересадки костного мозга и иммунодепрессантов прогноз стал в разы лучше.
Апластическая анемия
Под апластической анемией понимают группу патологических состояний, при которых наряду с панцитопенией обнаруживается снижение кроветворения в костном мозге и отсутствуют признаки гемобластоза. Апластическая анемия является скорее самостоятельной формой, а не синдромом. Из группы апластических анемий четко выделяется конституциональная анемия Фанкони. Среди большинства приобретенных апластических анемий выделяют формы с достаточно хорошо выученной этиологией. К таким относят апластические анемии, спровоцированные воздействием ионизирующей радиации либо вызванные приемом чрезмерно больших доз цитостатиков.
Особая группа апластических анемий возникает после острого вирусного гепатита. Описываются апластические анемии после приема лекарств, которые у большинства людей никаких изменений крови не вызывают. К таким препаратам относятся хлорамфеникол (левомицетин), фенилбутазон (бутадион), соединения золота, толбутамид (бутамид), сульфаметоксипиридазин (сульфапиридазин, кинекс), мепробамат (мепротан, андаксин триметадион (триметин), карбутамид (букарбан), хлорпромазин (аминазин).
Смертельная апластическая анемия бывает в 10 раз чаще у лиц, которые принимали левомицетин. Наиболее часто встречаются идиопатические формы апластических анемий, где при самом тщательном обследовании больного не удается выяснить причину болезни.
Что провоцирует / Причины Апластической анемии:
Принципиально возможны следующие механизмы развития апластической анемии: уменьшение количества стволовых клеток; нарушение микроокружения, приводящее к изменению функции стволовых клеток; внешние гуморальные или клеточные воздействия, в основном иммунные, нарушающие нормальную функцию стволовой клетки.
Ионизирующая радиация может вызвать апластическую анемию; она четко зависит от дозы радиации. При этом наблюдается гибель стволовых клеток.
Механизм развития аплазии после вирусной инфекции также недостаточно ясен. Аплазия развивается чаще после гепатита А или гепатита, не относящегося ни к группе А, ни к группе В. Описаны случаи аплазии после инфекционного мононуклеоза и 2 случая трансплантации костного мозга однояйцевым близнецам с постгепатитной аплазией. В одном случае отмечен эффект от трансплантации, в другом костный мозг не прижился; потребовалась подготовка циклофосфаном, а после нее трансплантация была удачной. Это не отвечает на вопрос, поражает вирус непосредственно стволовую клетку или существует гетероиммунный механизм развития аплазии (антитела против вируса, фиксированного на стволовой клетке, вызывают гибель этой стволовой клетки).
В пользу поражения стволовой клетки при апластических анемиях говорит эффективность трансплантации костного мозга от однояйцевых близнецов и братьев или сестер, совместимых по системе HLA.
Об иммунной природе апластической анемии у ряда больных свидетельствует отсутствие приживления трансплантированного костного мозга от однояйцевого близнеца без предварительной иммунодепрессии.
Симптомы Апластической анемии:
Клиническая картина идиопатической апластической анемии может быть разной. Иногда болезнь начинается остро и очень быстро прогрессирует, почти не поддается никакой терапии. Но чаще она начинается исподволь, больной адаптируется к анемии и обращается к врачу уже тогда, когда выраженность панцитопении значительная. Клиническая картина депрессии кроветворения складывается из анемии различной глубины, тромбоцитопении со всеми клиническими проявлениями тромбоцитопенического синдрома (такими как кровоподтеки, петехиальные высыпания на коже, носовые, десневые кровотечения, маточные кровотечения). Нередко следствием тяжелой нейтропении становятся пневмония, воспаление уха и другие воспалительные процессы. Иногда нагнаиваются ушибы, кровоизлияния, возможно инфицирование организма.
Анемия у больных связана как с нарушением образования эритроцитов, так и с кровотечениями.
Для таких больных характерна бледность, кожные кровоизлияния, достаточно специфичны воспалительные изменения на слизистой оболочке рта прямой кишки.
Врач при выслушивании сердца выявляет систолический шум. При идиопатической форме болезни селезенка не прощупывается. Ее увеличение отмечается уже при гемосидерозе в результате массивных переливаний эритроцитов. Увеличение печени может быть связано с недостаточностью кровообращения при анемии.
В одних случаях болезнь прогрессирует быстро и за несколько недель или месяцев приводит к смерти, в других – протекает хронически, с периодическими обострениями и улучшениями. Иногда наступает полное выздоровление.
Диагностика Апластической анемии:
Анемия выражена очень сильно, иногда гемоглобин снижается до 20-30 г/л. Анемия чаще нормохромная, макроцитарная. Содержание ретикулоцитов колеблется от 0 до 4-5%. Тяжелые формы сопровождаются большим снижением уровня ретикулоцитов. Эритрокариоциты в периферической крови появляются редко. Отмечается выраженная гранулоцитопения. Иногда количество гранулоцитов снижается до 0,2 Ч 109/л, при этом развиваются инфекционные осложнения. Иногда снижается абсолютное количество моноцитов. Абсолютный уровень лимфоцитов в большинстве случаев остается нормальным. Снижается количество тромбоцитов, при этом значительно удлиняется время кровотечения и, как следствие, развивается геморрагический синдром, СОЭ ускоряется до 30-50 мм/ч.
Количество миелокариоцитов костного мозга заметно снижается. Иногда отмечается раздражение красного ростка. Увеличено количество лимфоцитов, плазматических, тучных клеток. Мегакариоциты могут полностью отсутствовать. В костном мозге резко увеличивается количество железа, расположенного как в эритрокариоцитах, так и внеклеточно.
Содержание железа сыворотки у большинства больных увеличено, насыщение трансферрина приближается к 100%. При исследовании феррокинетики при помощи радиоактивного железа выявляются удлинение времени выведения железа из плазмы и снижение количества железа, включенного в эритроциты. Продолжительность жизни эритроцитов, измеренная при помощи радиоактивного хрома, чаще всего укорочена, реже – нормальная. Иногда повышается уровень фетального гемоглобина. Агрегатгемагглютинационная проба часто оказывается положительной. На поверхности эритроцитов выявляют IgG. Необходимо исключить присутствие аллоантител на поверхности недавно перелитых эритроцитов.
Диагностика апластической анемии возможна только после гистологического исследования костного мозга. Выявление панцитопении в периферической крови служит показанием к стернальной пункции (костномозговая пункция, производимая через переднюю стенку грудины) для исключения гемобластоза и витамин-В12-дефицитной анемии. После этого производится исследование взятого материала. При выявлении большого количества жира в костном мозге диагностируют апластическую анемию. Если при исследовании обнаруживается нормальное соотношение между кроветворной тканью и жиром или имеется структурное увеличение клеток, то диагноз апластической анемии отпадает. При этом нередко увеличивается селезенка, иногда бывает положительная проба Кумбса, но чаще антитела обнаруживаются при помощи агрегатгемагглютинационной пробы. В костном мозге — нормальное количество мегакариоцитов, тогда как при апластической анемии мегакариоциты почти полностью отсутствуют. При периферической панцитопении у пожилых людей, у лиц с удалением части желудка следует в первую очередь исключить витамин-В12-дефицитную анемию, у детей -фолиеводефицитную анемию.
К каким докторам следует обращаться если у Вас Апластическая анемия:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Апластической анемии, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .






