Супербактерии: не так уже и супер
После более чем 12 лет врачебной практики я внезапно из источника медицинской помощи превратился в активного пользователя последней. Попав в серьезную автомобильную аварию в 1986 году, я много месяцев провел на больничной койке, включая недели интенсивной терапии.
Находясь в палате интенсивной терапии, я был поражен одной из так называемых «супербактерий», которые являются бедой современных больниц. Супербактерии представляют собой род микробов, устойчивых практически ко всем (а в некоторых случаях ко всем без исключения) видам антибиотиков, известным человечеству.
Пара моих соседей по палате умерли от инфицирования этим паразитом. Бактериальный штамм поразил их иммунную систему и нарушил кровообращение, оставаясь невосприимчивым к самым дорогим и усовершенствованным антибиотикам.
Проблема «супербактерий» 1 все больше тревожит страны Запада. Эти микробы в первую очередь поражают высокотехнологичные больницы, занимающиеся наиболее серьезными заболеваниями. Применение дезинфицирующих средств в большем объеме не является решением проблемы; следует заметить, что некоторые виды паразитов обнаруживались именно в колбах с этими средствами! Чем больше антибактериального химического «оружия» идет в ход, тем более резистентными к нему становятся бактерии.
Реальность растущей устойчивости бактерий поначалу кажется явным признаком прогрессирующей эволюции. Но факты, после их тщательного изучения, показывают обратное.
Естественный отбор, а не эволюция
Эволюция – это, в сущности, идея того, что все создало себя самостоятельно —что природные процессы (на протяжении миллионов лет, без удивительного, божественного вмешательства) создали необыкновенно сложную совокупность существ. Согласно теории эволюции, было время, когда ни у одного существа в мире не было легких. Это означает, что не было генетической информации («программы» для живых существ, хранящейся в структуре молекул ДНК) для легких — нигде. Впоследствии «информация для легких» появилась и была добавлена в мир, но не было «информации для образования перьев»—перья появились позже.
Иными словами, для каждой особенности, возникающей вследствие эволюции, требовалась новая генетическая информация, которая добавлялась к общей информации в биосфере (т.е., ко всей информации, содержащейся во всех существах на земле). Некоторые особенности, разумеется, могут быть утеряны со временем, следовательно, не всегда наблюдается рост, но если микробы превратились в птиц, деревья и людей, требовалось серьезное увеличение объема информации. И речь идет не о беспорядочной смеси химических соединений, а о многозначительной информации, поскольку она отвечает за генетический код комплексных структур с важными функциями.
Поэтому если новая информация, новая функциональная сложность, может появляться сама собой там, где до этого ее не было, это может стать некоторой базой для идеи эволюции от молекул к человеку, хотя стопроцентной вероятности не будет. Однако, может быть так, что в каждой ситуации, когда популяции живых существ меняются, они делают это без увеличения (а часто и с уменьшением) объема информации. Таким образом, совершенно неправильно утверждать, что такие изменения демонстрируют «процесс эволюции». Разберемся, что известно о том, каким образом «супербактерии» стали устойчивыми, и зададим вопрос — возникли ли в процессе новые структуры или функции (либо другими словами, свидетельствовало ли что-либо об эволюции)?
Существует ряд способов, посредством которых у микробов может выработаться устойчивость к этим ядам. «Супербактерия» по своему определению устойчива ко множеству различных антибиотиков. Так, к антибиотику А резистентность может выработаться одним способом, к антибиотику B – совершенно другим, к антибиотику C – третьим. Так что если исследовать все известные способы формирования устойчивости в популяции микробов, можно увидеть, представляет ли собой какой-нибудь из них сложный процесс, вызывающий увеличение объема информации.
1. Некоторые бактерии уже изначально устойчивы.
Если из миллиона бактерий пять уже наделены особенностью, которая делает их невосприимчивыми (неважно каким способом эта особенность сформировалась), скажем, к пенициллину, тогда вымачивание в пенициллине убьет их всех, за исключением этих пяти. На сегодняшний день природная защита организма часто справляется с такой малочисленной популяцией до того, как та разрастется и причинит вред, следовательно, резистентность в таком случае не проблема. Однако, если организм потерпит неудачу, эти пять паразитов размножатся, и их потомство совершенно очевидно также будет резистентным. И через короткое время в организме будут миллионы микробов, равнодушных к пенициллину. Обратите внимание, что:
(i) Именно поэтому множественная резистентность к основному классу антибиотиков наиболее характерна для клиник, специализирующихся на более сложных заболеваниях—такие клиники часто используют усовершенствованную, дорогую «тяжелую артиллерию» антибиотиков, поэтому такого рода «естественный отбор» имеет место чаще.
(ii) В этом примере резистентная информация была уже заложена в популяции — она не появилась сама собой или же как реакция на антибиотик. То, что некоторые бактерии уже были невосприимчивы к изготовленным человеком антибиотикам еще до их изобретения – общеизвестный факт в кругах микробиологов. Образцы почвы из периферийной зоны, где современные антибиотики никогда не использовались, показали, что некоторые бактерии уже устойчивы к таким препаратам, как, например, метициллин, который никогда не существовал в природе. У бактерий, реанимированных из замороженных кишечников исследователей, которые погибли в полярных экспедициях, была выявлена устойчивость к ряду современных антибиотиков, еще не изобретенных на момент гибели исследователей. 2
2. Некоторые бактерии непосредственно передают свою устойчивость другим.
В удивительном процессе, имеющем в мире бактерий наибольшее сходство с совокуплением, один микроб вставляет крошечную трубку в другой, и маленькая петля ДНК – «плазмида» – передается от одного организма к другому. Такой способ генной передачи, посредством которой вполне очевидно может передаваться информация об устойчивости к лекарственному препарату, может быть осуществлен даже между разными видами бактерий.
Опять же, обратите внимание, что информация об устойчивости уже должна существовать в природе до момента ее передачи. Нет подтверждения факта возникновения чего-то совершенно нового, чего не существовало здесь до этого. Это передача информации, а не ее формирование.
Пока что мы имели дело со случаями, когда резистентность уже вполне очевидно существовала. Разумеется, эволюционисты бы утверждали, что подобная резистентность изначально появилась в (ненаблюдаемом) прошлом. Однако, если исследуемые изменения в настоящем не демонстрируют нам наличие новой информации, тогда что свидетельствует в поддержку идеи возникновения этой информации в прошлом? Механизмом, опережающим эволюцию, неизменно является мутация—ошибка копирования, случайное изменение в коде ДНК, переданное потомству. Это приводит нас к последнему способу формирования устойчивости в популяции бактерий.
3. Некоторые бактерии становятся устойчивыми путем мутации.
Любопытно, что там, где это происходит, нет четких признаков возникновения информации. Все виды мутации представляют собой потерю информации, дегенеративные изменения. Так, например, потеря контрольного гена может повысить степень устойчивости к пенициллину. 3
Некоторые антибиотики должны вводиться в бактерию, чтобы осуществлять свои функции. В бактериях имеются сложные химические насосы, которые могут активно всасывать питательные вещества извне через стенку клетки во внутреннюю часть бактерии. Бактерии, делающие это эффективно, при наличии одного из таких антибиотиков будут столь же эффективно проделывать это с ним, всасывая внутрь себя собственного убийцу.
Но что если один из этих микробов унаследует дефективный ген посредством ошибки копирования ДНК (мутации), который станет помехой эффективности работы химического насоса? И хотя этому паразиту будет не так просто выжить при нормальных обстоятельствах, такой дефект будет благоприятствовать его выживанию при наличии изготовленного человеком яда. 4 Мы снова видим, что информация утеряна / искажена, а не получена.
Супернеудачники
Именно потому, что мутации, стимулирующие устойчивость бактерий, являются дефектами в той или иной форме, так называемые ‘супербактерии’ на самом деле совсем не «супер»—они скорее «неудачники» по сравнению с их близкими родственниками. Когда меня, наконец, выписали из клиники, я все еще пребывал под разрушительным воздействием этих паразитов. Ничего не помогло от них избавиться, после столь долгого пребывания в больнице. Впрочем, как мне сказали, все, что нужно делать по приезде домой, это «подолгу находиться на улице, порой даже валяться в грязи, и ждать.» Менее чем через две недели супербактерии исчезли. Почему? Причина в том, что супербактерии в действительности дефективны несколько иначе, как объяснялось выше. Поэтому когда они вынуждены соперничать с обычными бактериями, которые по обыкновению живут на нашей коже, у них нет шансов. Они размножаются в клиниках, потому что все используемые там антибиотики и антисептики уничтожают обычные бактерии, которые при нормальных обстоятельствах были бы в состоянии вытеснить, уничтожить и вообще взять под контроль этих «супернеудачников». 5
Если они «слабее», тогда почему они становятся причиной смерти и страданий в больницах? Эти бактерии не более агрессивны, чем их сотоварищи, просто врачи имеют меньше возможностей остановить их. Кроме того, та среда, в которой по обыкновению «селекционируются» эти устойчивые микробы – например, палаты интенсивной терапии – это именно те места, где лежат критические больные, физически слабые и часто с открытыми ранами.
Поэтому не один микробиолог, обеспокоенный этими суперинфекциями, пришел к мысли (лишь с долей иронии), что лучшее, что можно сделать в главных клиниках – завалить коридоры кучей мусора, «нашпигованного» супербактериями, а не применять все больше и больше химикатов в бесконечной «гонке вооружений» против бактериального штамма. Иными словами, прекратить использование антибиотиков (что, конечно же, далеко не так просто), и вся эта «эволюция» изменит направление – популяции бактерий модифицируются, чтобы поддержать более выносливые, менее устойчивые виды.
Резюме и вывод
- «Супербактерии» в действительности не так уж нерушимы. Как правило, они менее выносливые и им сложнее выжить за пределами клиник.
- Существует множество примеров, когда бактерии становятся устойчивыми путем простой селекции резистентности, которая уже существовала ранее (включая «заимствованную» у других бактерий).
- Когда резистентность формируется вследствие мутационного дефекта, преимущество для выживания почти всегда обусловлено потерей информации. В таких случаях ничто не говорит о добавлении информации и о свидетельствующих о развитии изменениях.
- «Супербактерии» не свидетельствуют в поддержку постуляции, что живые существа превращались из простых в сложные путем добавления информации постепенно на протяжении миллионов лет.
Постскриптум
Смерть, страдания и болезни (включая инфекции) – часть проклятия, которое бременем легло на некогда совершенный мир в результате непослушания нашего прародителя Адама своему Создателю.
Фактически, бактерии свидетельствуют против эволюции. Их популяции размножаются с необычайной скоростью. Лишь за пару лет бактерии способны генерировать значительное число поколений, равносильное миллионам человеческих лет. Поскольку мы постоянно наблюдаем признаки мутации и естественного отбора в популяциях бактерий, мы должны видеть огромное количество признаков настоящей эволюции. Однако, на сегодняшний день нас по сути окружают те же самые виды, описанные Робертом Кохом столетие назад. Следует отметить, что существуют бактерии, найденные окаменелыми в каменных пластах и, по утверждению эволюционистов, насчитывающие миллионы лет, которые идентичны сегодняшним бактериям.
Известный французский биолог Пьер Грассе, много лет возглавлявший кафедру эволюции в Сорбонне, признал, что мутации бактерий просто демонстрировали перемещения туда и обратно с низкой степенью эффективности. Он резюмировал: «мутации не приводят ни к каким формам эволюции.» 6
Когда вы в следующий раз будете читать о «супербактериях», помните, что все, что о них известно, совпадает с заключенной в Книге Бытия идеей создания первоначально доброго, сложного мира, разрушенного грехом.
Ссылки и примечания
- Основные виды бактерий, устойчивых к множеству разновидностей антибиотиков одновременно (так называемая ‘множественная лекарственная резистентность’) – клебсиелла, пневмококк и стафилококк. Термин «золотой стаф» стал разговорным эвфемизмом для обозначения супербактерий, но, в сущности, это корректное выражение для обозначения наиболее распространенного вида стафа, известного еще как стафилококк ауреус или стафилококк пиогенес, также применяемое к бактериям, для которых множественная резистентность не характерна. Вернуться к тексту.
- R. McGuire, «Eerie: Human Arctic fossils yield resistant bacteria» (Макгуайер Р., Невероятно: в найденных в Арктике человеческих ископаемых обнаружены устойчивые бактерии), Medical Tribune December 29, 1988, pp. 1, 23. Вернуться к тексту.
- Ферментная пенициллиназа, вырабатываемая рядом бактерий, разрушает пенициллин. Если бы представитель бактериального штамма, продуцирующий небольшое количество этого вещества, унаследовал мутационный дефект, который разрушил или уничтожил ген, контролирующий производство фермента, организм потратил бы много ресурсов на производство большого количества пенициллиназы. Таким образом, этот дефект стал бы преимуществом в среде, содержащей пенициллин, но недостатком в других условиях. Опять же, налицо потеря информации. Нет доказательства того, что комплексная информация, отвечающая за генетический код производства пенициллиназы, сформировалась путем мутации. Вернуться к тексту.
- Для более детального и технического рассмотрения вопроса устойчивости к антибиотикам см. также C. Wieland, «Antibiotic Resistance in Bacteria» (Виланд К., Устойчивость бактерий к антибиотикам), CEN Technical Journal8(1):5–6, 1994. Вернуться к тексту.
- Разумеется, для медиков это настоящая дилемма, особенно в случае потребности пациента в антибиотиках для лечения болезней, которые вероятно излечить без их применения. Чем больше эти антибиотики используются, тем менее эффективными они становятся в некоторых жизнеопасных условиях. Вернуться к тексту.
- P-P Grasse, Evolution of Living Organisms (Грассе П. П., Эволюция живых организмов), Academic Press, New York, 1977, p. 88. Вернуться к тексту.
Карл Виланд, бакалавр медицины, бакалавр наук. Доктор Виланд является генеральным директором креационной организации ′Ответы в Книге бытия′ в Брисбене, Австралия. Он основал журнал Creation и является автором множества статей и докладов на тему мироздания и эволюции.
Все о супербактериях и как от них защититься
Видео: Супербактерии: типы, симптомы, лечение и профилактика
Содержание:
Супербаг. Похоже на возбужденного злодея, всей комической вселенной придется объединиться, чтобы победить.
Иногда — например, когда заголовки объявляют о непонятной вспышке, угрожающей крупному медицинскому центру, — это описание кажется устрашающе точным.
Но что современная наука может сказать о силе и уязвимости этих бактерий? И где мы находимся в борьбе за контроль над этими микроскопическими, но, казалось бы, непобедимыми противниками?
Продолжайте читать, чтобы узнать больше о супербактериях, угрозах, которые они представляют, и способах защиты от них.
Что такое супербактерии?
Супербаг это другое название бактерий или грибков, которые развили способность сопротивляться обычно назначаемым лекарствам.
Согласно отчету об угрозе устойчивости к антибиотикам за 2019 год, опубликованному Центрами по контролю и профилактике заболеваний (CDC), ежегодно в Соединенных Штатах происходит более 2,8 миллиона устойчивых к лекарствам инфекций, и более 35000 из них заканчиваются смертельным исходом.
Какие супербактерии вызывают наибольшее беспокойство?
В отчете CDC перечислено 18 бактерий и грибков, которые угрожают здоровью человека, классифицируя их как:
- срочный
- серьезный
- относительно угроз
Неотложные угрозы
- Карбапенем устойчивый Acinetobacter
- Candida auris
- Clostridioides difficile
- Carbapenem-устойчивые Enterobacteriaceae
- Лекарственно устойчивый Neisseria gonorrhoeae
Серьезные угрозы
- Лекарственно устойчивый Campylobacter
- Лекарственно устойчивый Candida
- Enterobacteriaceae, продуцирующие БЛРС
- Ванкомицин-устойчивый Энтерококки (VRE)
- С множественной лекарственной устойчивостью Синегнойная палочка
- Лекарственно-устойчивый нетифоидный Сальмонелла
- Лекарственно устойчивый Сальмонелла серотипа Typhi
- Лекарственно устойчивый Шигелла
- Метициллин-устойчивый Золотистый стафилококк (MRSA)
- Лекарственно устойчивый Пневмококк
- Туберкулез с лекарственной устойчивостью
Об угрозах
- Эритромицин-резистентная группа А Стрептококк
- Клиндамицин-резистентная группа B Стрептококк
Каковы симптомы заражения супербактериями?
У некоторых людей заражение супербактериями вообще не вызывает никаких симптомов. Когда здоровые люди переносят микробы без симптомов, они могут заразить уязвимых людей, даже не осознавая этого.
N. gonorrhoeaeНапример, это бактерии, передающиеся половым путем, которые часто остаются незамеченными, потому что не сразу проявляют симптомы.
Однако при отсутствии лечения гонорея может нанести вред нервной системе и сердцу. Это может вызвать бесплодие и внематочную беременность, которые могут быть опасными для жизни.
Относительно недавно, N. gonorrhoeae эволюционировал, чтобы выдержать лечение цефалоспорином, антибиотиком, который когда-то был золотым стандартом для уничтожения организма.
Когда инфекции супербактериями действительно проявляются, они сильно различаются в зависимости от того, какой организм атакует вас. Общие симптомы инфекционного заболевания включают:
- высокая температура
- усталость
- понос
- кашляющий
- боли тела
Симптомы заражения супербактериями выглядят так же, как симптомы других инфекций. Разница в том, что симптомы не поддаются лечению антибиотиками и противогрибковыми препаратами.
Кто подвергается риску заражения супербактериями?
Заразиться супербактериями может любой человек, даже молодой и здоровый. Вы можете подвергаться повышенному риску заражения, если ваша иммунная система была ослаблена хроническим заболеванием или лечением рака.
Если вы работаете в медицинском учреждении или недавно проходили лечение в больнице, амбулатории или реабилитационном центре, возможно, вы контактировали с бактериями, которые более распространены в медицинских учреждениях.
Если вы работаете в ветеринарном учреждении или в сельском хозяйстве, вы можете столкнуться с супербактериями в процессе работы.
Некоторые супербактерии передаются с пищей, поэтому вы можете подвергнуться риску заражения, если ели зараженные продукты или продукты от животных, которых лечили антибиотиками.
Как лечится инфекция супербактерий?
Если у вас инфекция супербактерия, ваше лечение будет зависеть от того, какие бактерии или грибки вызывают инфекцию.
Ваш врач может отправить образец вашего тела в лабораторию, чтобы лаборанты могли определить, какой антибиотик или противогрибковый препарат эффективен против супербактерии, вызывающей ваше заболевание.
Новая наука в контратаке супербактерий
Исследования лекарственно-устойчивых инфекций являются актуальной задачей во всем мире. Это два из многих достижений в борьбе с этими ошибками.
- Исследователи из Швейцарского университета Лозанны обнаружили 46 препаратов, Пневмококк от входа в состояние, называемое «компетенцией», в котором он может захватывать генетический материал, плавающий в окружающей среде, и использовать его для развития сопротивления. Эти нетоксичные препараты, одобренные FDA, позволяют бактериальным клеткам жить, но не позволяют им генерировать пептиды, которые запускают состояние эволюционной компетентности. До сих пор эти препараты работали на моделях мышей и в клетках человека в лабораторных условиях. Приведенная выше ссылка на исследование включает пояснительное видео.
- Исследования, проведенные в Университете Квинсленда, Австралия, показали, что 30 соединений, содержащих серебро, цинк, марганец и другие металлы, были эффективны по крайней мере против одного бактериального штамма, один из которых был устойчивым к метициллину супербактерий. Золотистый стафилококк (MRSA). Отчеты показывают, что о 23 из 30 соединений ранее не сообщалось.
Как можно предотвратить заражение супербактериями?
Как бы угрожающе ни звучали супербактерии, есть способы защитить себя и свою семью от заражения им. CDC рекомендует:
- тщательно вымойте руки
- сделай прививку своей семье
- используйте антибиотики с умом
- соблюдать особые меры предосторожности с животными
- практиковать безопасное приготовление пищи
- заниматься сексом с презервативом или другим барьерным методом
- немедленно обратитесь за медицинской помощью, если вы подозреваете инфекцию
- держите раны чистыми
- позаботьтесь о себе, если у вас хроническое заболевание
Когда обратиться к врачу
Если ваш врач лечит вас от инфекции, но ваши симптомы не улучшаются после того, как вы закончили прием лекарств, вам следует немедленно обратиться к врачу.
Медицинские работники клиники Мэйо рекомендуют вам посетить врача, если:
- у тебя проблемы с дыханием
- ты кашляешь больше недели
- у вас сильная головная боль, боль в шее и скованность, а также жар
- вы взрослый человек, у вас температура выше 103 ° F (39,4 ° C)
- у вас внезапно возникла проблема со зрением
- у вас сыпь или отек
- тебя укусило животное
Ключевые выводы
Супербактерии — это бактерии или грибки, которые развили способность противостоять обычно назначаемым лекарствам.
Супербактерии могут заразить кого угодно, но некоторые люди могут иметь более высокий риск заражения, потому что они подверглись воздействию супербактерий в медицинском учреждении или имеют ослабленную иммунную систему из-за хронического заболевания.
Люди, которые работают в ветеринарных учреждениях или с животными, особенно в агробизнесе, также подвергаются большему риску.
Супербактерии можно переносить без симптомов. Если у вас есть симптомы, они будут различаться в зависимости от того, какой инфекцией вы заразились.
Если ваши симптомы не поддаются лечению, это может быть связано с тем, что вы заразились лекарственно-устойчивым супербактериальным микробом.
Глобальная проблема XXI века: «супербактерии» против человечества
Одной из наиболее сложных задач для ученых сегодня может стать поиск путей решения проблемы устойчивости к антибиотикам патогенных бактерий. Наука ищет выходы из ситуации, и кое-что уже придумано. Способ борьбы с «супербактериями» разрабатывают и отечественные ученые из Госкорпорации Ростех. Подробнее о производстве альтернативных лекарственных средств – в материале, опубликованном на научно-популярном портале Naked Science .
Как известно, в 2014 году в Женеве Всемирная организация здравоохранения сделала доклад, содержащий полную картину влияния традиционных антимикробных препаратов на бактерии с учетом данных полученных из 114 стран. Картина получилась неутешительная: традиционные лекарственные препараты, включая антибиотики, оказались бесполезны либо слабы в отношении различных переносчиков инфекции. Явление назвали «антимикробной резистентностью».
В 2017 году ВОЗ опубликовала список критической группы бактерий, представляющих собой повышенную опасность. В их числе – Acinetobacter baumannii, синегнойная палочка (Pseudomonas aeruginosa), энтеробактерии (Enterobacteriaceae), энтерококки фэциум (Enterococcus faecium), золотистый стафилококк (Staphylococcus aureus), хеликобактер пилори (Helicobacter pilori), кампилобактеры (Campylobacter), сальмонелла (Salmonella), гонококк (Neisseria gonorrhoeae), пневмококк (Streptococcus pneumonia), гемофильная палочка (Haemophilus influenza), шигелла (Shigella).
В числе устойчивых микроорганизмов оказались также бактерии Klebsiella pneumonia, Escherichia coli, MRSA (метициллин устойчивые бактерии Staphylococcus aureus) и другие, вызывающие серьезные заболевания: сепсис, гонорею, инфекции мочевыводящих путей, пневмонию.
Так, к примеру, по данным ученых ВОЗ, случаи бесполезного лечения гонореи цефалоспоринами третьего поколения, относящихся к группе антибиотиков повышенной активности и применяющихся в качестве «крайней меры», подтвердились в десяти странах. Случаи зарегистрированы в Австралии, Австрии, Канаде, Норвегии, Словении, Швеции, Франции, Южной Африке, Японии и Соединенном Королевстве. Это притом что в мире этим заболеванием ежедневно инфицируется более одного миллиона человек.
Также, по оценкам ВОЗ, вероятность смерти людей инфицированных MRSA на 64% выше, если сравнивать с неустойчивой формой инфекции. Кроме того, по данным доклада центра RANDEurope и KMPG, от устойчивых к антибиотикам инфекций в мире ежегодно умирает по меньшей мере 700 тысяч человек. В США, по данным американского Центра по контролю и профилактике заболеваний, эта цифра ежегодно составляет 23 тысячи человек, в Евросоюзе показатель достигает 25 тысяч.
Зарождение «супербактерии»
Для того чтобы понять, почему микроорганизмы становятся устойчивыми к лекарствам, важно знать их природу. Бактерии представляют собой одну из первых форм жизни на Земле. Ископаемые свидетельства датируются в ряде случаев началом периода архея – 3,5 миллиарда лет назад. Это обширная группа одноклеточных микроорганизмов.
И чтобы понять, как появляются «супербактерии», вспомним биологию, точнее, ее раздел, посвященный синтетической эволюции. Как известно, ее основополагающие принципы – естественный отбор, наследственность и изменчивость. Согласно теории, новые признаки в строении организмов и их функциональных особенностях возникают в связи с изменчивостью, которая, в свою очередь, может быть определенной и неопределенной.
Первый тип изменчивости имеет место, когда условия окружающей среды оказывают одинаковое влияние на всех особей одного вида. Примером такой изменчивости может послужить появление у зайцев белой шерсти, что ожидаемо в зимний период, поскольку это помогает быть более незаметными для хищников на снегу. Такой тип изменчивости затрагивает фенотипические особенности организма и не наследуется генетически.
Неопределенная изменчивость напрямую связана с изменениями генотипа организма, которые, как правило, нельзя предугадать. Пример – индивидуальные мутации, возникшие у отдельных особей одного вида. Подобная изменчивость может проявляться вне зависимости от текущих условий окружающей среды и способна устойчиво передаваться потомству.
Вспомним и о наследовании приобретенных признаков, открытом еще французским биологом Жаном Батистом Ламарком, основной тезис которого заключается в том, что в ответ на изменения окружающей среды организмы способны меняться, приспосабливаться и передавать приобретенные изменения своему потомству.
По форме бактерии можно разделить на палочковидные – бациллы, сферические – кокки – и спиралевидные – спириллы. По своему строению бактерии делятся на прокариот (доядерные), ДНК (дезоксирибонуклеиноваякислота) которых находится в определенной зоне клетки бактерии, и эукариот (ядерные) – их ДНК располагается в окруженном оболочкой ядре клетки.
Но, несмотря на разнообразие форм и строения, все бактерии объединяет одно важное свойство – способность передавать из поколения в поколение информацию с помощью своего генетического материала (ДНК), в том числе об устойчивости к лекарственным средствам. Причем передача информации и проявление новых признаков, включая резистентность, могут происходить достаточно быстро, учитывая скорость размножения бактерий.
Многие из них путем деления способны давать потомство в течение 30 минут, а за сутки всего одна клетка может образовать 72 новых поколения, каждое из которых получает определенную информацию об устойчивости к лекарственным препаратам, если, конечно, прародитель сталкивался с тем или иным антимикробным средством.
В результате такой передачи информации через некоторое время может появиться поколение «супербактерий», которые являются невосприимчивыми ни к одному известному антибиотику, как в случае с 70-летней американкой из штата Невада. В 2017 году женщина скончалась из-за полной резистентности бактерии Klebsiella pneumoniae к 26 видам известных антибиотиков. Все они оказались полностью бесполезны в борьбе с инфекцией.
Наука и устойчивость
В настоящее время наиболее известными средствами для борьбы с бактериями являются антибиотики, появлению которых мировое сообщество обязано Александру Флемингу, обнаружившему в 1928 году в ходе исследования, что обыкновенная плесень Penicillium, которая произрастает на лежалом хлебе, вырабатывает вещество, убивающее бактерии семейства Staphylococcaceae. Так появился всем известный «пенициллин».
Сегодня в мире существует несколько тысяч натуральных и даже синтетических антибиотиков, объединенных в 16 классов. Например, пенициллин, относится к бета-лактамным препаратам. Но из всего множества созданных ранее антибиотиков в настоящее время используется не более пяти процентов. Это напрямую связано с тем, что бактерии со временем выработали устойчивость к основной массе таких препаратов.
Все это побудило ВОЗ после проведенных масштабных исследований с 2014 года рассматривать проблему антимикробной резистентности на глобальном уровне и рекомендовать мировому научному сообществу приступить к поиску путей ее решения.
У ученых есть много идей, как справиться с проблемой: изучение механизмов возникновения антимикробной резистентности и системный мониторинг ее распространения, совершенствование мер по ограничению распространения и циркуляции возбудителей с антимикробной резистентностью). Среди них есть и такой метод борьбы – научиться выращивать устойчивые виды бактерий и исследовать химические соединения, с помощью которых резистентность будет преодолена.
Эту задачу, в частности, решают ученые Северо-Восточного университета в Бостоне (США). Им удалось найти ряд соединений, к одному из которых в лабораторных условиях ни одна из исследуемых бактерий не способна была выработать устойчивость.
И если речь идет, например, о создании принципиально нового вида антибиотиков, то необходимо понимать, что на их разработку, прохождение всех этапов исследований и внедрение в массовое производство, по данным экспертов, уходит в среднем 10 лет. В этой связи ученые также ищут способы решения глобальной проблемы на базе альтернативных антибиотикам противомикробных средств.
Если говорить о нашей стране, то в 2017 году для этих целей была утверждена «Стратегия предупреждения распространения антимикробной резистентности в Российской Федерации на период до 2030 года». Она предусматривает меры по ограничению распространения устойчивости микроорганизмов к противомикробным препаратам, химическим и биологическим средствам.
В частности, стратегия интегрирует в себя план действий по разработке и внедрению альтернативных методов, технологий, средств профилактики и лечения заболеваний, включая создание биологических лекарственных препаратов на основе бактериофагов.
Вирусы против «супербактерий»
Бактериофаги – это не новый биологический вид. Научное сообщество приступило к их изучению задолго до появления всем известных антибиотиков. Первые научные сообщения о бактериофагах появились еще в 1920-х годах.
В 1921 году Ричард Брайонг и Джозеф Мэйсин, последователи Феликса Д’Эрреля, французского микробиолога и первооткрывателя бактериофагов, сделали доклад об успешном лечении инфекций кожи стафилококковым бактериофагом, а в 1922 году Д’Эррель в своем фундаментальном труде изложил результаты начального этапа изучения бактериофагов. И только в 1929 году Александр Флеминг открыл пенициллин.
Кроме того, в романе американского писателя Синклера Льюиса «Эроусмит» про молодого микробиолога, вышедшего в 1925 году, также говорилось о новом методе лечения: изобретенная ученым сыворотка губительно действовала на бактерии и спасла множество жителей Карибских островов от эпидемии бубонной чумы. По сути, речь шла о фаготерапии.
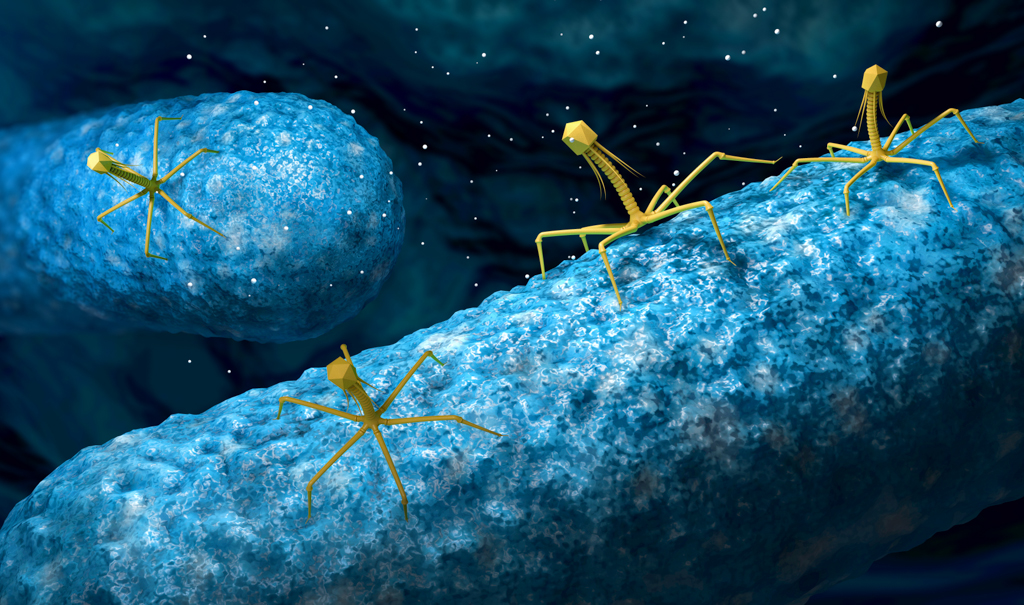
Что же такое бактериофаги? Они представляют собой внеклеточную форму жизни. Иными словами, это вирусы, размеры которых составляют в среднем от 20 до 200 нанометров (1 нанометр равен одной миллиардной части метра). Так же, как и бактерии, эти вирусы представляют собой еще одну наиболее распространенную форму жизни на нашей планете. Они присутствуют буквально везде: в океане, почве, глубоководных источниках, питьевой воде, пище.
Причем бактериофаги способны размножаться исключительно в клетке-хозяине. Они могут иметь кубическую, нитевидную или форму головастиков. Любая фаговая частица состоит из головки, содержащей нуклеиновую кислоту (ДНК или РНК), заключенную в белковую оболочку – капсид, – и хвостового отростка, состоящего из внутреннего стержня и сократительного чехла. Передвигается бактериофаг с помощью ножек-фибрилл, скрепленных в центре базальной пластиной.
Все бактериофаги имеют особенность, которой и пользуются ученые в ходе создания альтернативных антибактериальных препаратов – каждому типу бактерий свойственны собственные вирусы-фаги. При этом бактериофаги, как снайперы, избирательно поражают только бактериальные клетки, а не всю микрофлору организма, в отличие от антибиотиков.
Происходит этот процесс в несколько этапов. Сначала бактериофаг распознает бактериальную клетку и прикрепляется к ее оболочке. Затем вирус-бактериофаг производит инъекцию своей нуклеиновой кислоты (генома) внутрь бактерии. Далее происходит биосинтез белковых и нуклеиновых компонентов новых фаговых частиц на основе введенного генома. Еще один этап – соединение компонентов и формирование новых бактериофагов внутри бактерии. И, наконец, процесс лизиса – распад бактериальной клетки и выход зрелых фагов.
Иными словами, эти неклеточные формы жизни с генетической программой способны проникать практически в любую вредоносную бактериальную клетку, размножиться и разрушить ее, не причиняя вреда остальной микрофлоре организма. Подобный «литический цикл» продолжается до тех пор, пока не будет уничтожена последняя бактерия.
При неблагоприятных внешних условиях и малом количестве вредоносных клеток бактериофаги развиваются по лизогенному циклу: введенный геном существует внутри клетки пассивно – не размножаясь.
В таком состоянии «зараженная» фаговым геномом бактерия может проходить циклы деления. И когда такая бактерия попадет в благоприятные для размножения вируса условия, вновь активизируется литический цикл развития бактериофагов.
Кроме того, в отличие от антибиотиков, бактериофаги способны приобретать новые признаки естественным образом для борьбы с резистентными мутациями бактериальных клеток.
Отечественные разработки
Если говорить об успехах отечественных ученых в создании альтернативных антимикробных препаратов на основе бактериофагов, то еще благодаря сотрудничеству Феликса Д’Эрреля и грузинского микробиолога Георгия Элиавы в 1920-х годах в СССР был создан первый и единственный в мире научно-исследовательский центр бактериофагологии.
Уже в 1930-х бактериофаги советского производства впервые были использованы в экстренных ситуациях. Например, в 1938 году в нескольких пограничных с СССР районах Афганистана для профилактики эпидемии холеры бактериофаги давали местному населению, добавляли в колодцы и водоемы. В результате на советской территории не было зарегистрировано ни одного случая заболевания.
Во времена Великой Отечественной войны также применялась фаговая терапия. Особое внимание уделялось разработке и производству бактериофагов, подавляющих кишечные инфекции – холеру, брюшной тиф, дизентерию и сальмонеллез. Всего за годы войны для фронта было изготовлено более 200 тысяч литров бактериофагов.
В наши дни в России разработкой и производством альтернативных лекарственных средств на основе бактериофагов в рамках Стратегии по борьбе с антимикробной резистентностью занимаются ученые НПО «Микроген» холдинга «Нацимбио» (входит в Госкорпорацию Ростех).
В настоящий момент предприятие приступило к созданию всероссийской базы штаммовой коллекции бактериофагов для выпуска новых лекарственных противомикробных препаратов на их основе.
На сегодняшний день НПО «Микроген» разработаны 19 разновидностей альтернативных лекарственных противомикробных препаратов на основе бактериофагов против дизентерии, брюшного тифа, сальмонеллеза, гнойно-септических и других заболеваний.
В перспективе – выпуск первого в мире лекарственного препарата, содержащего бактериофаги в капсулах для лечения и профилактики заболеваний, вызываемых бактериями рода стафилококков (лат. Staphylococcus), стрептококков (Streptococcus), протеи (Proteus – P. vulgaris, P. mirabilis), клебсиеллы (Klebsiella pneumoniae), синегнойной (Pseudomonas aeruginosa) и кишечной (Escherichia coli) палочек.
Кроме того, в 2018 году предприятие приступило ко второй фазе клинических исследований бактериофага «Дифаг», направленного на борьбу с бактериями рода Acinetobacter baumannii (ацинетобактер) и Pseudomonas aeruginosa (синегнойная палочка), которые наиболее часто вызывают инфекционные заболевания у пациентов хирургических стационаров, отделений реанимации и интенсивной терапии.
Результаты наработок зарубежных и российских ученых по поиску новых антимикробных средств, безусловно, вселяют уверенность в том, что глобальная задача антимикробной резистентности в скором времени может быть решена. А пока каждый из нас остается участником развернувшейся в XXI веке невидимой глазом битвы между человечеством и «супербактериями».
Рейтинг 12 самых опасных супербактерий

Вы могли никогда не слышать о таких микроорганизмах как акинетобактерия Баумана, синегнойная палочка, или энтеробактерии. Но эти три убийцы возглавили официальный список бактерий, для которых крайне необходимы новые лекарства. Он был составлен Всемирной организацией здравоохранения (ВОЗ) и содержит 12 бактерий и бактериальных семейств. Причем наименования из топ-3 входят в критически опасную категорию.
Рейтинг самых опасных супербактерий не предназначен для того, чтобы напугать людей. Это сигнал для исследователей и фармацевтических компаний о том, каковы должны быть их приоритеты.
Вот как выглядит полная подборка устойчивых к антибиотикам микроорганизмов, ранжированных по приоритету важности от среднего до критического.
12. Пневмококки
Устойчивость: к пенициллину
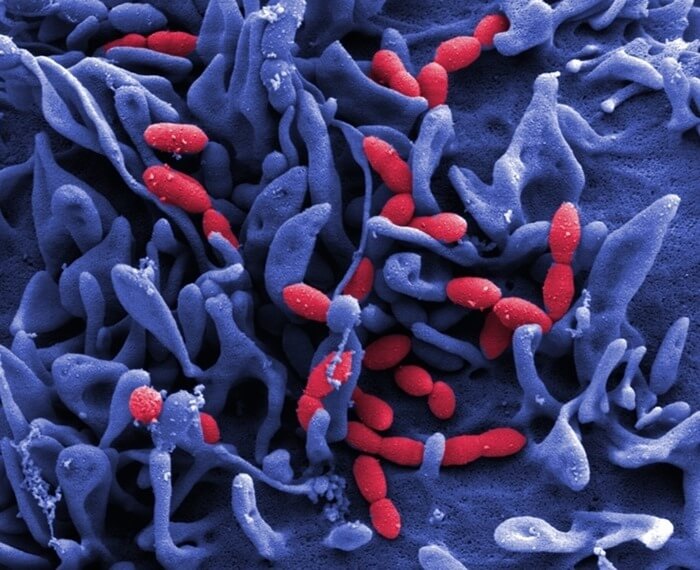
Эти бактерии могут стать причиной многих видов заболеваний, в том числе: пневмонии (воспаление легких), инфекций уха и пазух, менингита (инфекции оболочек головного и спинного мозга), и карбункула (заражение крови). Пневмококковые бактерии распространяются через кашель, чихание и тесный контакт с инфицированным человеком.
11. Гемофильная палочка
Устойчивость: к ампициллину
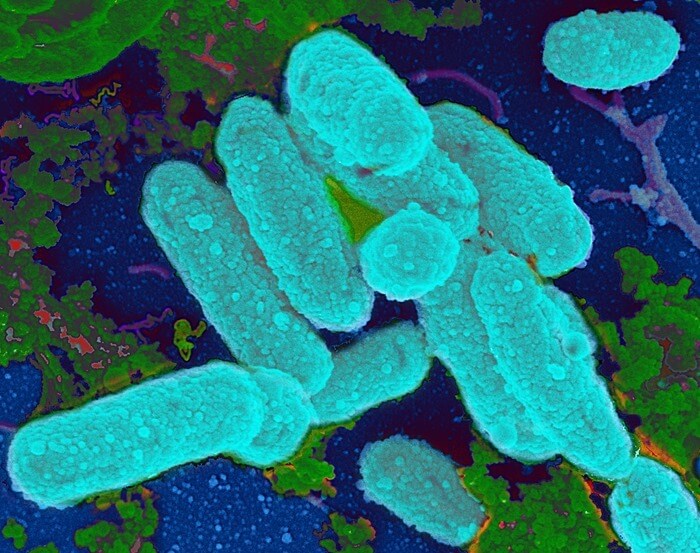
Эти микроорганизмы могут вызывать инфекции у людей всех возрастов, начиная от легких, таких как инфекции уха, до тяжелых, такие как инфекции кровотока.
10. Шигеллы
Устойчивость: к фторхинолону
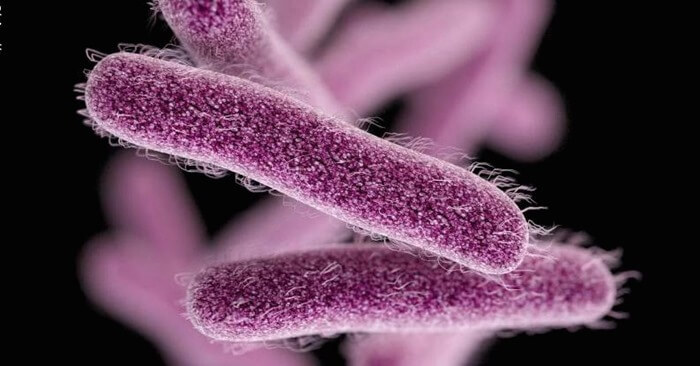
Эта группа бактерий вызывает заболевание под названием шигеллез. Большинство больных шигеллезом жалуются на понос, лихорадку и спазмы желудка. Дизентерия обычно длится от 5 до 7 дней. Избежать этого заболевания можно с помощью частого и тщательного мытья рук с мылом и соблюдения правил гигиены.
9. Энтерококки фэциум
Устойчивость: к ванкомицину
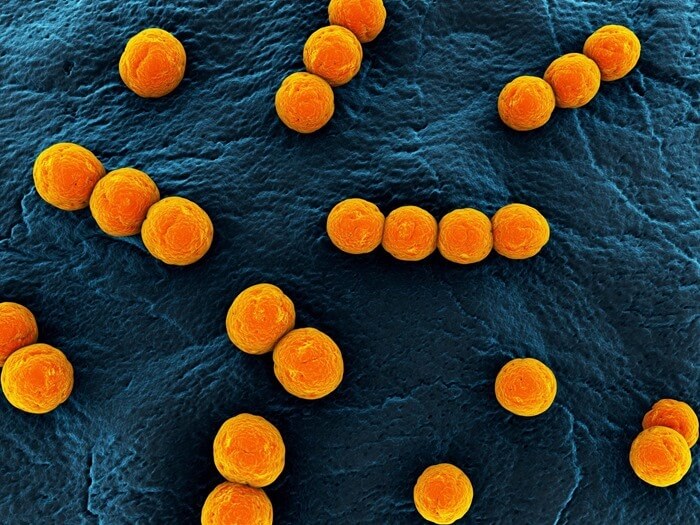
Энтерококки являются частью нормальной кишечной флоры у большого числа млекопитающих, и в настоящее время эти микробы используются в качестве индикаторов
загрязнения фекалиями воды и пищевых продуктов. Эти организмы считаются одной из основных причин внутрибольничных и инфекционных заболеваний из-за способности выжить в окружающей среде и их внутренней устойчивости к противомикробным препаратам. Часто вызывают инфекции мочеполовых органов.
8. Золотистый стафилококк
Устойчивость: к метициллину, нейтральный и устойчивый к ванкомицину
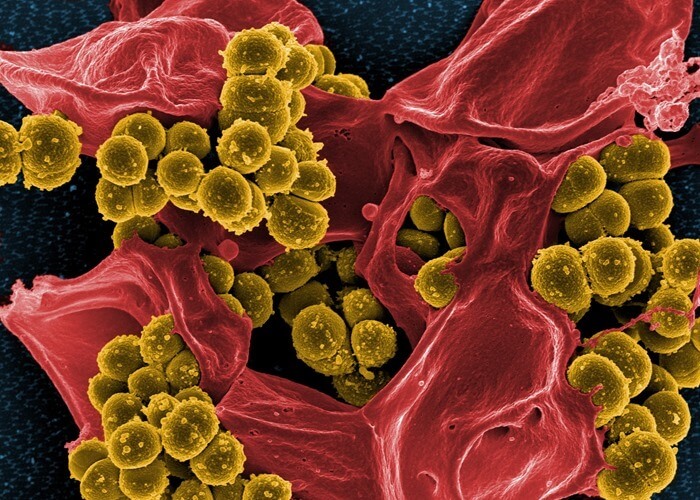
Этот патоген вызывает широкий спектр клинических инфекций. Это ведущая причина инфекционного эндокардита, а также кожных и плевролегочных инфекций.
7. Хеликобактер пилори
Устойчивость: к кларитромицину
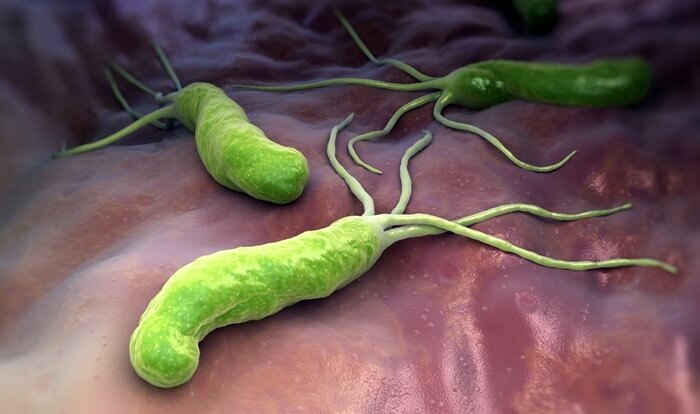
В 2005 году была доказана связь между этой бактерией и возникновением язвы желудка и кишечника. Этот микроорганизм, размером в 3 мкм, единственный из своих «собратьев» способен выживать и размножаться в кислой среде желудочного сока.
6. Кампилобактеры
Устойчивость к фторхинолону
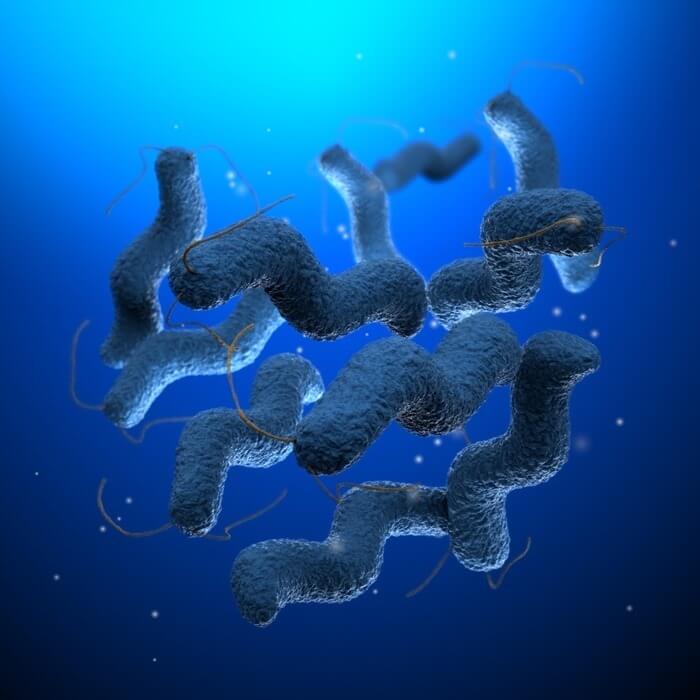
На шестом месте в рейтинге опаснейших бактерий, невосприимчивых к антибиотикам, находятся микроорганизмы из рода Campylobacter. Они вызывают кампилобактериоз — инфекционное заболевание, сопровождающееся диареей, спазмами, болями в животе и лихорадкой. Диарея может быть кровавой и «дополняться» тошнотой и рвотой. Болезнь обычно длится около недели
5. Сальмонелла
Устойчивость: к фторхинолону
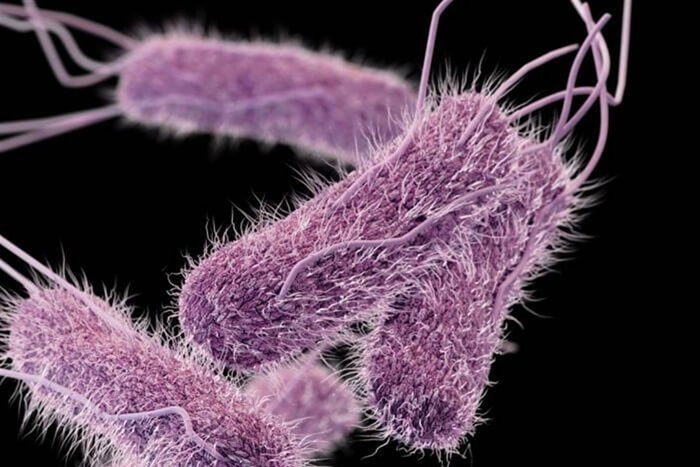
У людей, инфицированных сальмонеллой, развивается диарея, лихорадка, боль в животе спустя от 12 до 72 часов после заражения. Большинство людей выздоравливают без лечения через 4-7 дней. Тем не менее у некоторых больных диарея может быть настолько сильной, что их приходится госпитализировать.
4. Гонококки
Устойчивость: к фторхинолону и цефалоспорину
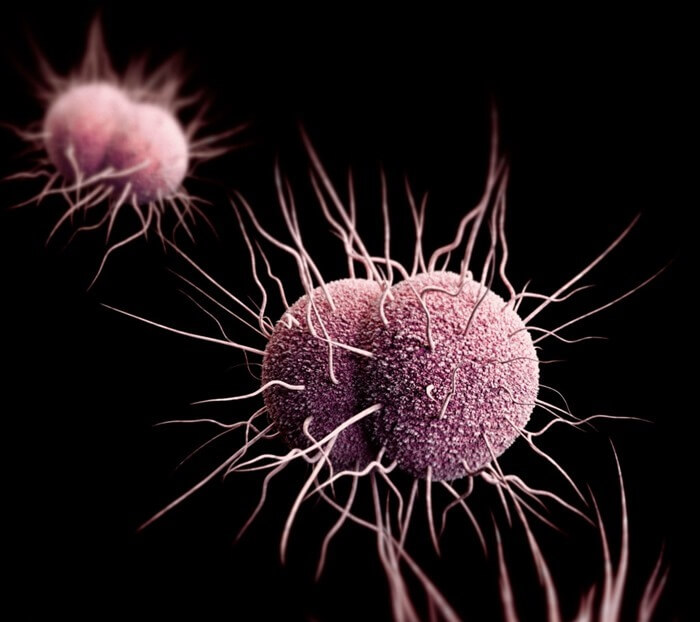
Именно эти бактерии следует «благодарить» тем, у кого возникла гонорея. Ну и еще сексуального партнера, так как гонорея передается в основном половым путем (другой путь передачи — через личные вещи).
3. Акинетобактерия Баумана
Устойчивость: к карбапенемам
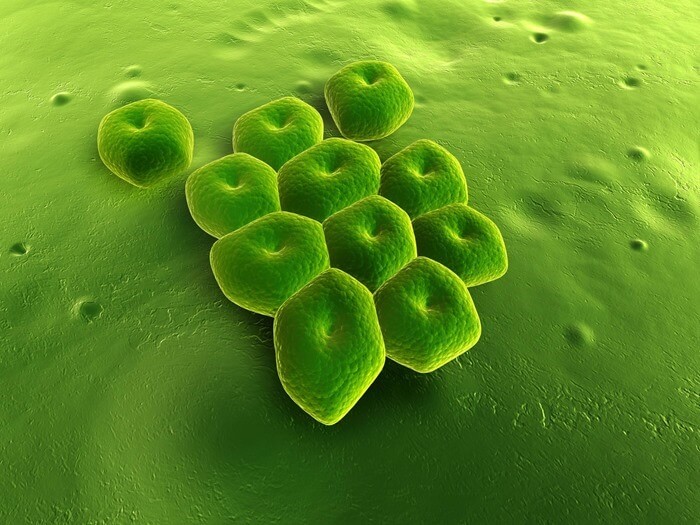
Acinetobacter baumannii — важнейший представитель рода Acinetobacter — является одним из наиболее опасных патогенов для учреждений здравоохранения во всем мире. Он обладает способностью быстро приобретать устойчивость к антибиотикам, что делает его одной из важнейших супербактерий, угрожающих нынешней антибиотической эре. Самой распространенной инфекцией, вызванной этим микробом, является госпитальная пневмония.
2. Синегнойная палочка
Устойчивость: к карбапенемам
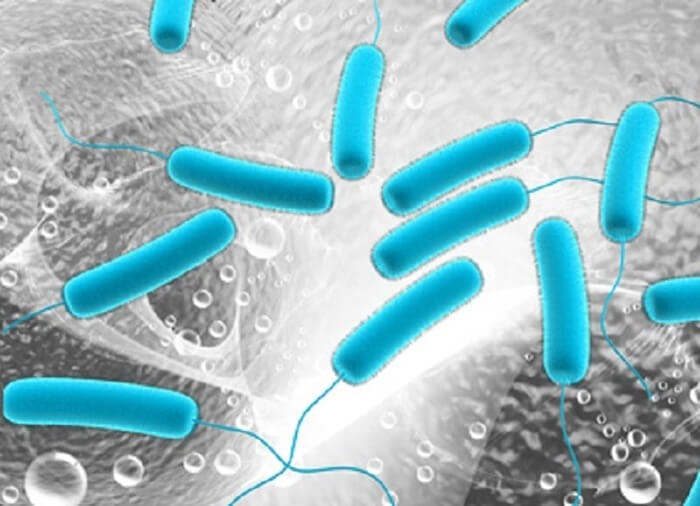
Патоген, поражающий пациентов со слабым иммунитетом. Синегнойная палочка известна как основная причина заболеваемости и смертности у пациентов с муковисцидозом и как одна из ведущих причин внутрибольничных инфекций
1. Энтеробактерии, в том числе клебсиелла, кишечная палочка, серрации и протеус
Устойчивость: к карбапенемам и штаммам, продуцирующим бета-лактамазы расширенного спектра действия
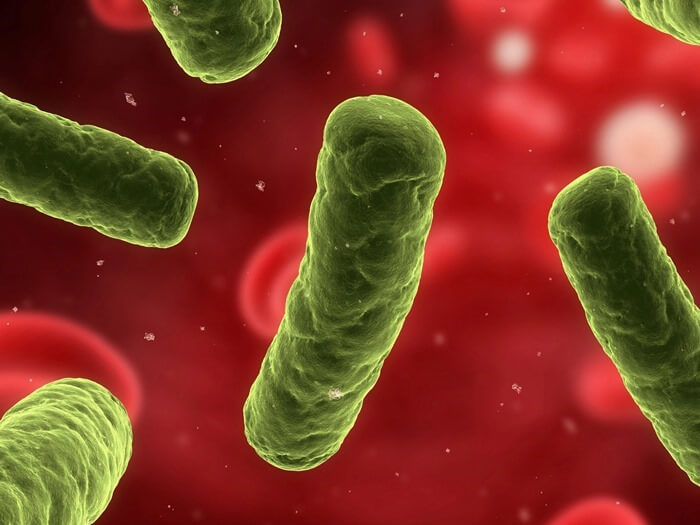
Как и предыдущие два участника списка опаснейших бактерий современности энтеробактерии относятся к грамотрицательным бактериям, устойчивым ко многим лекарственным препаратам. Они не широко распространены, но вызывают серьезные, часто смертельные инфекции, особенно у людей с ослабленным иммунитетом, например, в результате химиотерапии или трансплантации органов. Наиболее опасные штаммы недавно приобрели устойчивость к классу антибиотиков под названием «карбапенемы». Это были единственные лекарства, которые ранее эффективно убивали энтеробактерии, синегнойную палочку и акинетобактерию Баумана.
Один патоген, с устойчивостью к антибиотикам, не вошел в подборку ВОЗ. Речь идет о микобактерии туберкулеза. Проблема туберкулеза с лекарственной устойчивостью хорошо известна, а цель рейтинга ВОЗ заключалась в том, чтобы акцентировать внимание на угрозах, которые еще не получили широкого признания.
Супербактерии и бактериофаги: чем заменить антибиотики?
Что такое супербактерии? К чему приводит бесконтрольное самолечение? Почему антибиотики больше не панацея, чем их заменить и как работают бактериофаги? На эти вопросы в интервью Sibnet.ru ответила завлабораторией молекулярной микробиологии ИХБФМ СО РАН Нина Тикунова.
Массовое производство и применение антибиотика началось с пенициллина, в 1943 году. Препараты, способные убивать бактерии, спасли человечество от множества инфекционных болезней. Однако, по данным ВОЗ, практически все существующие патогенные бактерии приобретут устойчивость к антибиотикам уже через 10-20 лет. И если сейчас из-за устойчивости к антибиотикам ежегодно не удается спасти 700 тысяч человек, то к 2050 году число жертв бактериальных инфекций возрастет до 10 миллионов в год.
— Известно, что антибиотики совершили революцию…
— Да, антибиотики приносили огромную пользу людям, и их стали активно использовать не только в медицине, но и в других областях: в сельском хозяйстве — птицеводстве и скотоводстве; в производстве предметов гигиены — зубная паста, мыло, средства обработки помещений.
Как работает антибиотик? В норме бактерии постоянно живут в нашем организме, в кишечнике их около 1,5 килограмма, в целом бактерий в человеке больше, чем собственных клеток. Но если человек подхватывает вирус или испытывает длительный стресс, его иммунитет снижается, и эти бактерии начинают активно размножаться, что приводит к ухудшению самочувствия. Также существуют инфекционные заболевания, вызываемые бактериями.
Остановить размножение бактерий, уничтожить их и вылечить человека могут антибиотики. Эти лекарства спасли много людей.
— И что изменилось?
— Конкретному человеку полезна паста с антибиотиками, она спасает его от определенного количества бактерий. Но когда сточная вода со всего города, от птицефабрик и свиноферм попадает в воду и почву, с этими антибиотиками сталкиваются бактерии. Они находят способы выживания — развивается антибиотикорезистентность (устойчивость бактерий к антибиотикам).
Антибиотикорезистентность возникла потому, что многие почвенные бактерии несут в себе гены устойчивости к антибиотикам. Эти гены путем горизонтального переноса (когда генетический материал передается организму — не потомку) могут с невысокой вероятностью перейти от одного вида бактерии к другому.
Сначала бактерии стали невосприимчивы к одним антибиотикам, а затем появились супербактерии — бактерии с множественной устойчивостью к антибиотикам, — от которых не спасает уже целый ряд антибиотиков.
Были случаи, когда пациентов не успевали вылечить до того, как выясняли, к какому именно антибиотику чувствительна заразившая их бактерия.

— Врачи, столкнувшись с этим явлением, договорились, что определенную группу лекарств используют только в крайних случаях, это препараты резерва, «последнего ряда».
В нее ВОЗ включила восемь препаратов, таких как колистин, и некоторые антибиотики из группы цефалоспоринов. Как только их начнут бесконтрольно принимать, к ним тоже разовьется антибиотикорезистентность.
— Правильно ли, что запретили свободную продажу антибиотиков?
— Да, самолечение опасно, после приема антибиотиков у человека может выработаться резистентность и в случае сильного заболевания трудно будет подобрать действенный препарат, так как бактерии ко многим из них приспособятся.
За рубежом — в Европе, США и Канаде — это правило действует очень строго. Но зачастую пока пациенты дождутся несколько дней, чтобы попасть к врачу, заболевание разгорается сильнее, чем если бы его начали лечить в самом начале.
В этом плане российская медицина выигрывает. Если у нас в отделение клещевых инфекций попадает человек с подозрением на боррелиоз (температура после укуса клеща и т.д.), его сразу начинают лечить антибиотиками. То есть наши врачи не допускают развития тяжелых форм заболевания. За рубежом не так. Сначала больного обследуют, а вдруг у него нет боррелиоза, начинают лечить с опозданием, в итоге там много случаев тяжелейшего развития этой болезни.
— ВОЗ в 2005 году провозгласила постантибиотиковую эру. Что это значит?
— Это означает прекращение безусловной веры в помощь антибиотиков и необходимость поиска альтернативных средств. Человек — существо разумное, многочисленное, хорошо приспосабливающееся к изменению внешних условий. Думаю, человечество что-то изобретет.
Фармкомпании из-за антибиотикорезистентности вернулись к разработке новых антибиотиков, рассматривают альтернативные препараты. Но новые антибиотики создать сложно, так как ученые за многие десятилетия разработали антибиотики на ключевые точки процесса размножения бактерий.
Часть заболеваний можно вылечить без антибиотиков. Один из альтернативных вариантов — использование бактериофагов.
— Можно ли совсем отказаться от антибиотиков?
— Запретить сейчас полностью использование невозможно. Иначе мы столкнемся с голодом и смертями.
Так, в США запретили вводить антибиотики в средства гигиены. Но современное сельское хозяйство не может существовать без антибиотиков.
В медицине большая часть инфекционных заболеваний пока успешно лечится ими, в клиниках берут анализ на чувствительность к антибиотикам, и врач применяет нужный препарат.
Но если человека привозят, например, с заражением крови, его срочно надо лечить, то сразу применяют антибиотики широкого спектра действия и параллельно делают анализ на чувствительность той бактерии, которая является причиной инфекции. Если лекарство правильно подобрано, то продолжают лечение, либо меняют.
— Вы сказали, что часть болезней можно лечить бактериофагами, что это?
— Бактериофаги — древние вирусы, пожирающие бактерии. Если бы их не было, то за двое суток Земля покрылась бы толстым слоем бактерий. Бактериофаги, как и другие вирусы, вне хозяина никакой деятельности не развивают – не живут, то есть не размножаются.
Каждый фаг убивает только определенную группу бактерий и никак не действуют на другие, например, на нормальную кишечную и кожную микрофлору, в отличие от антибиотиков.
Поскольку фаги никак не заражают клетки человека и животных, они не приносят вреда организму. За время эволюции человечество к ним приспособилось, и иммунная система на них не реагирует отрицательно, нет токсического эффекта. Поэтому их можно давать новорожденным, больным с аутоиммунным заболеваниями и онкологией.

— И они полностью смогут заменить антибиотики?
— Рассчитывать, что они спасут человечество вместо антибиотиков, нельзя. Избирательность бактериофагов как их плюс, так и минус. Штаммов бактерий в мире сотни тысяч, а бактериофаги подобраны только на десятки или сотни.
В каждом случае нужно время, чтобы подобрать бактериофаг для больного с помощью анализа. Поэтому острые бактериальные инфекции надо быстро гасить антибиотиками. Бактериофаг нужен при заболеваниях, вызванных супербактериями или в случае хронических бактериальных заболеваний.
Фаги отлично дополняют антибиотики и даже помогают им уничтожить врага. Бактерии в ране зачастую образуют многослойную биопленку, в которую антибиотик пробиться не может. Бактериофаг, действуя на одну из бактерий, пробивает «броню» этой пленки и делает возможным действие антибиотика.
— Уже разработаны какие-то препараты бактериофагов, от каких заболеваний?
— В нашей стране еще в советское время начали успешно использовать препараты бактериофагов. Только в России крупные фармацевтические компании («Микроген») производят препараты бактериофагов. Это не БАДы, а терапевтические препараты, прошедшие стадии доклинических и клинических испытаний.
Спектр заболеваний большой — бактериальные кишечные заболевания, их лечение актуально для детей, у которых из-за бактериальных диарей происходит быстрое обезвоживание, а применение антибиотиков не всегда желательно. Это спектр раневых инфекций и послеоперационных воспалений, ЛОР-заболеваний, хронических стоматологических заболеваний, диабетическая стопа (язвы на стопах — осложнение диабета, ведущее к ампутации).
— Как назначаются эти препараты?
— Они есть в свободной продаже. Врачи, работавшие в 60-80-е годы, знали и широко использовали бактериофаги. Вероятно, сейчас в мединституте этим знаниям уделяют немного внимания. Большинство современных врачей о них или не знают, или забывают.
Несмотря на то, что это не БАД, они не включены в списки обязательных медицинских препаратов, которые должны быть в государственной больнице, поэтому врачи в этих медучреждениях не могут их использовать, в отличие от частных.
Бактериофаги используют частные клиники, больные сами ищут информацию, часто нам звонят, спрашивают. Мы объясняем, что надо обратиться в лабораторию, сделать анализ на антибиотикорезистентность и чувствительность к бактериофагу.
— Как создаются препараты бактериофагов, если они такие узконаправленные?
— Чаще всего создаются коктейли из бактериофагов. Они направлены на один вид бактерий, например, на стафилококки, но покрывают широкий спектр штаммов (вариантов стафилококков). Также есть коктейли бактериофагов против разных видов бактерий. Это для экстренного лечения. Часто использовать одни и те же коктейли нельзя — может развиться устойчивость к бактериофагам.
— Какова ваша роль в создании новых бактериофагов?
— У нас научно-исследовательский институт. Главная задача — находить новые и необычные бактериофаги. Мы ищем их в образцах от больных и здоровых людей, в природных образцах, в том числе из экстремофильных мест обитаний – вечная мерзлота, соленые и термальные озера.
Интересный объект — стоки птицефабрик и свиноферм. Можно найти необычные гены, что поможет создать новые инструменты синтетической биологии. То есть найти подходы и способы лечения, позволяющие проводить нужные манипуляции с геномом — разрушить геном вредного (вирус, раковые клетки) или создать геном полезного (клетки, синтезирующие лечебное вещество).
Например, чтобы бактериофаги разрушали именно тот штамм, который у пациента, надо повысить его специфичность. Или у специфичного, но не очень эффективного фага, повысить эффективность.
В нашей коллекции несколько сотен бактериофагов и несколько тысяч образцов штаммов бактерий. Каждый новый бактериофаг мы проверяем, на какие бактерии он действует.
Если к нам обращаются врачи-клиницисты, присылают образцы, мы можем подобрать подходящие бактериофаги.
По международному соглашению сейчас, если все одобренные средства лечения не помогают улучшить состояние больного, медики проводят консилиум и с согласия пациента имеют право использовать официально неодобренные препараты.
Например, при диабетической стопе пациенты соглашаются на лечение бактериофагами, потому что могут избежать ампутации. Мы либо подбираем в аптеке препараты, которые хорошо действуют, либо ищем из своей коллекции.
В 30-40% случаев используем штаммы аптечных фагов, еще в 30-40% из нашей коллекции, в 20-25% не можем подобрать бактериофаг. За пять-шесть лет поучаствовали в излечении более сотни больных.
Также мы создали свой коктейль против 11 редких бактериальных агентов, как раз против супербактерий. В том числе он помогает от диабетической стопы. Но пока препарат не проходил испытания даже на животных, потому что на это надо десятки миллионов рублей.
— А за рубежом используют бактериофаги?
— Зарубежный мир всегда пренебрежительно относился к советской науке, тем более к медицине. В последние годы, осознав, что в ряде случаев бактериофаги, использовавшиеся советскими медиками, могут быть спасением, они тоже стали ими заниматься.
И боюсь, европейские и американские ученые в ближайшее время опередят нашу страну, которая с 30-х годов производит препараты бактериофагов, но не так широко их используют.
Проблема в разработке и выпуске на рынок бактериофагов еще в том, что любой микробиолог, купив в аптеке коктейль бактериофагов, может размножить их в лаборатории. И эта особенность тормозит желание фармкомпаний вкладывать деньги в выпуск таких препаратов.
Я думаю, выход из этой ситуации в том, что фармкомпании будут вставлять в геном коммерческих фагов какой-то штрих-код, чтобы потом недобросовестные конкуренты не могли использовать чужие фаги.
— Есть ли еще варианты замены антибиотиков кроме бактериофагов?
— Да, есть. Бактерии выделяют пептиды, чтобы убавить количество конкурентных неродственных им видов в одном сообществе. Ученые ищут способ использовать эти пептиды против бактерий. И эти исследования активно развиваются.
Что за супербактерия клебсиелла пневмонии и помогут ли от нее антибиотики?
В соцсети Twitter появились сообщения о супербактерии, которую не может «убить» ни один из предлагаемых для лечения антибиотиков. Один из белорусских пользователей продемонстрировал результаты анализа на чувствительность к клебсиелле пневмонии (Klebsiella pneumoniae): на фото бланка видно, что напротив названия каждого из 24 антибиотиков, которыми возможно лечение, стоит буква «R», обозначающая резистентность (устойчивость).
С аналогичной ситуацией не раз сталкивались и зарубежные медики. Так, в 2017 году американские ученые обнаружили у более чем трети обследованных пациентов клиник Хьюстона редкий штамм этой супербактерии, который оказался устойчивым к действию большинства используемых в Соединенных Штатах антибиотиков.
В том же году в прессе появилась информация о гибели в США 70-летней пациентки после заражения супербактерией Klebsiella pneumoniae: врачи не смогли спасти женщину, потому что бактерия оказалась устойчива ко всем 26 антибиотикам, которые могли использоваться для лечения. В итоге больная скончалась от сепсиса (заражения крови). А в 2012 году газета The Washington Post сообщала о том, что в госпитале Национальных институтов здравоохранения в результате вспышки инфекции, вызванной стойким к антибиотикам штаммом Klebsiella pneumoniae, умерли шесть пациентов.

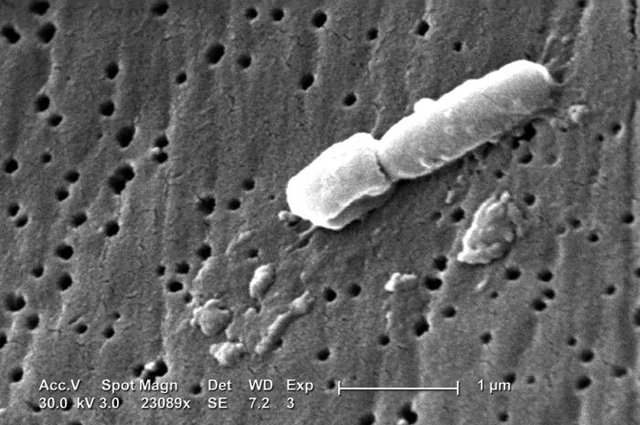
Что за бактерия клебсиелла пневмонии и чем она опасна?
Речь идет об анаэробной палочковидной бактерии из рода клебсиелл, которая повсеместно встречается в окружающей среде, в том числе в почве и поверхностных водах. Клебсиеллу открыл в 1882 году микробиолог из Германии Карл Фридлендер, поэтому ее второе название — палочка Фридлендера. Эта условно-патогенная бактерия живет в организме человека, совершенно никак себя не проявляя, пока сохраняется здоровый баланс и поддерживается оптимальная микрофлора. Опасной она становится лишь тогда, когда «хорошие» бактерии ослабевают или их количество резко уменьшается.
Палочка Фридлендера может вызывать различные патологии, включая сепсис, инфекции мочевыводящих путей, бактериемию, менингит и абсцессы в печени. Довольно часто клебсиелла является причиной острой пневмонии. Инфицированию чаще всего подвержены люди с иммунодефицитами, тяжелыми сопутствующими заболеваниями и ослабленной иммунной системой.
Особенно опасной для человека является Klebsiella pneumoniae (клебсиелла пневмонии). Она является преобладающим возбудителем внутрибольничной инфекции в ряде стационаров. Источником инфекции, как правило, служит больной человек или бактерионоситель. Наиболее частые пути передачи — пищевой, воздушно-капельный и контактно-бытовой.
Где можно заразиться клебсиеллой пневмонии и смогут ли от нее вылечить?
«Klebsiella pneumoniae в настоящее время все чаще и чаще является возбудителем инфекции внутри стационара. Она в числе так называемых внутрибольничных инфекций. Бактерия приобретает сегодня множественную резистентность к большинству современных антибиотиков. Но правда состоит в том, что большинство механизмов резистентности уже осознаны, и в настоящее время создаются новые антибактериальные препараты, которые преодолевают эту резистентность. Да, конечно, клебсиелла представляет угрозу, если вовремя не понять, что инфекция вызвана ей. В таком случае все может закончиться плохо. Но если мы точно знаем, что причиной заболевания является эта бактерия, и знаем ее механизмы резистентности, то у медиков есть определенные возможности, чтобы с ней побороться. Все не совсем так безнадежно», — говорит врач, клинический фармаколог, заведующий кафедрой общей и клинической фармакологии РУДН Сергей Зырянов.
Почему клебсиелла становится все более устойчивой к антибиотикам?
Бактерии все чаще приспосабливаются к антибиотикам и передают ген устойчивости другим бактериям, таким образом появляются супербактерии. Это возбудители инфекционных болезней, которые устойчивы сразу к нескольким антибиотикам, традиционно использующимся для лечения данных заболеваний. Способность супербактерий противостоять антибиотикам вызывает озабоченность в мировом сообществе, проблему даже обсуждают на уровне Генеральной Ассамблеи ООН.
«Так, к сожалению, происходит, что все микробы, которые обитают в стационарах, становятся более устойчивыми и резистентными, поскольку в медицинских организациях при лечении часто назначают антибиотики. Микробы от этого становятся более устойчивыми к различным воздействиям, и врачам приходится применять больше сил, больше затрат, связанных с лечением такой инфекции», — говорит Зырянов.
В отличие от других бактерий Klebsiella обладает способностью образовывать капсулу, что делает ее устойчивой во внешней среде. Такая капсула предохраняет возбудителя от высыхания, поэтому клебсиеллы могут долгое время сохраняться при комнатной температуре. Большинство штаммов Klebsiella pneumoniaе невосприимчивы к пенициллинам, цефалоспоринам III-IV поколений, аминогликозидам, фторхинолонам.

Как ранее отмечали американские врачи, особая проблема заключается в том, что некоторые штаммы клебсиеллы также стали более устойчивы к антибиотикам группы карбапенемов. Эти лекарства ранее считались наиболее эффективными при лечении инфекций, вызванных Klebsiella pneumoniae, но в последние годы стали терять эффективность.
Какие существуют способы лечения Klebsiella pneumoniae?
По словам Зырянова, нельзя говорить о том, что на клебсиеллу не действует ни один из антибиотиков. Существуют новые антибактериальные препараты, которые созданы специально для того, чтобы преодолеть резистентность клебсиеллы. Чтобы получить эффект от лечения, также применяют комбинацию уже известных препаратов.
Терапевтический эффект может иметь лечение большей дозой антибиотиков, но все зависит от конкретного штамма бактерии, конкретного антибиотика и состояния пациента. «Увеличение дозы, в зависимости от конкретного антибиотика, может оказать воздействие на бактерию. Также это зависит от того, о каком штамме клебсиеллы идет речь. Есть определенные показатели резистентности, если они позволяют это делать, то тогда таким способом пользуются. В ряде случаев увеличение дозы действительно помогает», — говорит Зырянов.
Кроме того, врач отмечает, что вне больницы заразиться этой супербактерией практически невозможно. «Клебсиелла пневмонии, которая обладает экстремальной лекарственной резистентностью, во внебольничных условиях практически не существует. Это госпитальный возбудитель», — говорит он.
Что такое супербактерии рэш
Некоторые бактерии — настоящие супермены в своем микромире. Они завоевывают новые территории, успешно справляются с разработанным против них оружием в виде антибиотиков и постоянно совершенствуют свои способности. А мы, то есть человечество, пока медленно, но верно проигрываем эту битву. MedAboutMe выяснял, кто такие супербактерии и в чем причина их успеха?
Супербаги — ошибки или успех эволюции?
В СМИ для обозначения не поддающихся действию антибиотиков бактерий все чаще используется слово «супербаги». Когда-то о «багах» (жучках — от англ. bugs), имея в виду мелкие ошибки, говорил еще Томас Эддисон. А на заре программирования англоязычное словечко bug стали активно использовать разработчики в области компьютерных технологий. Для программиста баг — это ошибка в программе или в системе, приводящая к неожиданным результатам.
В 1966 году появились первые сообщения о лекарственно-устойчивых бактериях, которые могут передавать это свойство другим видам микробов. Журналисты окрестили их супербагами — микроорганизмами-ошибками, которые приводят к очень неожиданным результатам с точки зрения врачей и ученых. Но на самом деле, ошибками их называть неправильно, потому что появление супербактерий — результат их борьбы за выживание в мире, в котором на каждом шагу применяются антибиотики. Так что это, скорее, очередной шаг по лестнице эволюции, чем баг.
Как супербактерии защищаются от антибиотиков?

Изобретательность супербактерий в создании способов защиты от антибиотиков вызывает невольное восхищение. Вот лишь некоторые способности, которые развили у себя бактерии за несколько десятков лет борьбы с антибиотиками:
- умение вырабатывать специальный фермент, который разрушает действующее вещество антибиотика;
- умение создавать барьер, через который антибиотик проникнуть не в состоянии;
- изменение соединения-мишени, на контакт с которой рассчитан антибиотик.
Но главная головная боль ученых, которые пытаются остановить эпидемию превращения рядовых бактерий в супербагов — это горизонтальный перенос генов.
Дело в том, что у бактерий генетический материал может существовать в виде плазмид — небольших участков закольцованной ДНК. Бактерии умеют обмениваться этими плазмидами и таким образом могут передавать гены другим микроорганизмам, которые не являются их потомками. Более того, речь может идти о переносе генов между разными видами. Это все равно, как если бы человек мог передать часть своей ДНК при помощи рукопожатия или, например, погладив собаку. Сам процесс горизонтального переноса генов был открыт в 1959 году японскими учеными в ходе изучения процесса передачи свойства резистентности к определенным антибиотикам от одного вида микробов к другим. Сегодня встречаются супербаги, несущие в себе не одну, а множество плазмид с генами устойчивости к разным антибиотикам. Особенно часто такие супербактерии появляются в больницах, где обмен генами и вопросы борьбы с антибиотиками стоят у бактерий особенно остро.
Гены, которые делают из обычных бактерий супербагов

В ходе войны бактерий за выживание появляются гены, которые придают микроорганизмам суперсвойства, передаваемые от микроба к микробу, от одного вида к другому путем горизонтального переноса. Сегодня ученым известно о существовании следующих генов, которые делают из бактерий супербагов.
Ген, защищающий от бета-лактамов
Фермент с громоздким названием «металло-бета-лактамаза из Нью-Дели» (NDM-1) кодируется геном, открытым относительно недавно. Бактерии, обладающие им, неуязвимы к подавляющему большинству бета-лактамных антибиотиков — пенициллинам, цефалоспоринам и карбапенемам. А ведь еще недавно бета-лактамы, которые нарушали процесс образования клеточной стенки бактерий, считались самыми универсальными антибиотиками, и потому применялись особенно широко. Причем карбапенемы использовались для борьбы с особо стойкими больничными инфекциями.
Только монобактамы из этой группы пока еще «держат оборону». Единственный бета-лактамный антибиотик, способный устоять перед действием NDM-1 — азтреонам. Но и он не всесилен и разрушается под действием бета-лактамаз расширенного спектра (ESBL-ферментов). Микроорганизмы, обладающие генами, которые кодируют ESBL-ферменты, тоже встречаются уже довольно часто.
Сегодня ген NDM-1 обнаружен у отдельных штаммов кишечной палочки (Escherichia coli) и клебсиелл (Klebsiella pneumoniae).
Ген, защищающий от «антибиотиков последней надежды»
Менее двух лет назад у американки с неизлечимым циститом были обнаружены возбудители инфекции с геном MCR-1, при наличии которого бактерия получает устойчивость сразу к множеству лекарств, включая «антибиотики последней надежды». Так ученые называют полимиксины — группу полипептидных антибактериальных средств, из которых наиболее известным является колистин. Это препарат «глубокого резерва», его обычно назначают, когда бактерия оказывается устойчивой ко всем остальным антибиотикам.
Ген MCR-1 также входит в состав плазмиды, которая с легкостью необыкновенной передается между разными видами бактерий путем горизонтального переноса. Благодаря этой легкости, за период с ноября 2015 года, когда его впервые обнаружили, по настоящее время ген уже успел проявиться в более чем 30 странах, расположенных на 5 континентах.
В список бактерий, где его находили, вошли: кишечная палочка (E.coli), один из видов сальмонеллы (Salmonella enterica), клебсиелла (Klebsiella pneumonia) и пара энтеробактерий (Enterobacter aerogenes и E. cloacae). В лаборатории ученые наблюдали также передачу плазмиды с геном от кишечной палочки к синегнойной — возможно, прямо сейчас где-то в мире этот процесс происходит в организме живого человека.
Что нас ждет?

Итак, количество супербактерий растет. В прошлом году в этом списке появилась новая запись — энтеробактерии, устойчивые к карбапенемам (CRE). Том Фриден (Tom Frieden), бывший глава системы американских Центров по контролю и профилактике заболеваний (CDC), назвал их «бактериями из ночных кошмаров». Из разных концов мира приходят сообщения о новых случаях обнаружения супербагов, которых сложно, а то и невозможно, уничтожить с помощью традиционных антибиотиков.
Это значит, бактерии, даже те, что уже обзавелись эффективными средствами защиты, продолжают эволюционировать, подстраиваясь под постоянно меняющиеся условия и достижения фармакологии. И первоочередная задача человечества — решить проблему резистентности к антибиотикам, пока супербаги не начали убивать людей массово. В противном случае антибиотики могут стать бесполезными. Когда-то они совершили революцию в медицине, и даже теперь, на современном уровне развития здравоохранения, отказ от них может оказаться для нас тяжелым ударом.
Поэтому основная работа ученых сегодня ведется в двух направлениях:
- Поиск принципиально иных методов борьбы с бактериальными инфекциями.
- Ограничение использования антибиотиков там, где это возможно.
И именно поэтому так важно не принимать антибиотики без назначения врача, а если требуется пропить курс — строго следовать его указаниям. Только совместными усилиями можно замедлить скорость появления супербагов.






